Electrostimulator perineal pentru incontinență Beac IntelliSTIM BE-28UG
- Peste 90.000 de clienți mulțumiți din 2020
- Plăți securizate: card de credit, PayPal și transfer bancar
- Expediere accelerată: Poste, BRT, FedEx
- Suport clienți Whatsapp +39 371 43 61 201
Electrostimulatorul perineal BECA 28UG este o unitate terapeutică pentru tratamentul incontinenței, prin electrostimulare perineală, pentru uz profesional sau personal.
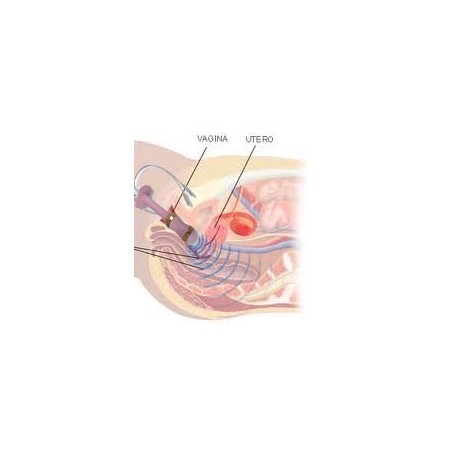
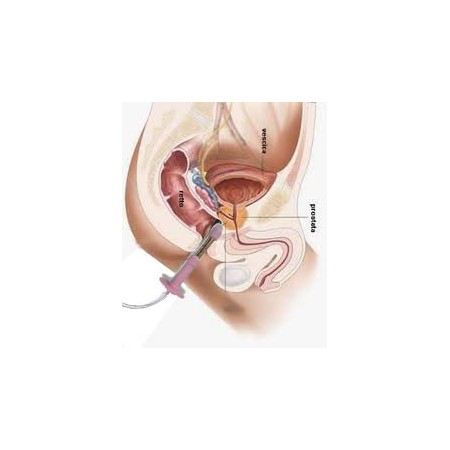
Electrostimularea perineală Intellistim 28UG BEAC, folosind sonde vaginale sau anale, reprezintă tratamentul de elecție în numeroase cazuri de incontinență urinară.
Posibilitatea integrării tratamentului profesional cu sesiunile la domiciliu este adesea crucială pentru succesul terapeutic.
Unitatea IntelliSTIM UG, deși este echipată cu caracteristici sofisticate și flexibilitate funcțională, necesare pentru uz profesional, este și ușor de utilizat direct de către pacient.
- Ecran LCD mare
- Utilizare simplă și intuitivă
- 4 programe gratuite
- 11 programe selectabile, potrivite pentru diferite tratamente pentru incontinență.
- Funcția IntelliSTIM cu reglare interactivă automată a parametrilor de timp
- Afișarea tuturor parametrilor și posibilitatea modificării în timpul sesiunii
- 2 forme de undă selectabile pentru utilizare cu sonde inelare sau cu tijă.
Aparatul este capabil să efectueze, prin achiziționarea electrozilor, stimulare tibială pentru tratamentul problemelor pelvine.
Stimulare electrică transcutanată neinvazivă în tratamentul vezicii urinare hiperactive
Abstract
Am analizat literatura de specialitate privind stimularea electrică transcutanată a nervilor (TENS) utilizată ca terapie pentru simptomele vezicii hiperactive (OAB), cu accent deosebit pe: locul stimulării, parametrii stimulului, structurile neuronale considerate a fi vizate și rezultatele clinice și urodinamice obținute. Majoritatea studiilor au utilizat stimularea nervului sacral sau tibial. Literatura de specialitate sugerează că, deși terapia TENS poate avea efecte neuromodulatoare, este puțin probabil ca pacientul să beneficieze semnificativ de o singură aplicare a TENS și, într-adevăr, nu au fost raportate beneficii clare din studiile acute. În studiile pe termen lung au existat diferențe în descrierile intensității stimulării, strategiei terapeutice și plasării electrozilor, precum și în diversele simptome și patologii ale pacienților. În plus, majoritatea studiilor au fost necontrolate și, prin urmare, nu au evaluat efectul placebo. Se cunosc puține lucruri despre mecanismul de bază prin care funcționează aceste terapii și, prin urmare, despre exact ce structuri trebuie stimulate și cu ce parametri. Există dovezi promițătoare privind eficacitatea unei abordări de stimulare transcutanată, dar va fi necesară o standardizare adecvată a criteriilor de stimulare și a măsurilor de evaluare a rezultatelor pentru a defini cea mai bună modalitate de a gestiona această terapie și de a documenta eficacitatea acesteia.
1. Introducere
Simptomele sindromului vezicii hiperactive (OAB) reprezintă un set bine cunoscut de simptome pe care pacienții le resimt în timpul fazei ciclului urinar. Se caracterizează prin urgență (o dorință bruscă și imperioasă de a urina, dificil de amânat) care, la aproape toți pacienții, este însoțită de creșterea frecvenței și nicturie și, în special la pacientele de sex feminin, de incontinență de urgență. [1] . Aproximativ o treime dintre pacientele de sex feminin suferă de incontinență urinară severă. [2] .
Stimularea electrică a fost utilizată timp de câteva decenii în tratamentul diferitelor disfuncții ale tractului urinar inferior. Stimulatorul sacral anterior radicular Finetech-Bridley Consolidated [3] , o rădăcină sacrală electrică implantată (S 2 -S 4 ) stimulator pentru a ajuta la golirea vezicii urinare, a format un precursor al tehnicilor populare de neuromodulație sacrală de astăzi [4]] și [5 ] . Eu S. 2 -S 4 Rădăcinile nervoase asigură alimentarea vezicii urinare cu principiul motor. În special S. 3 Rădăcina inervează în principal mușchiul detrusor și este ținta principală a neuromodulației sacrale.
Un alt loc de stimulare important și bine stabilit este cel al nervului tibial posterior (PTN). PTN este un nerv mixt care conține L 5 -S 3 fibre, din nou provenind din aceleași segmente spinale ca și inervațiile parasimpatice ale vezicii urinare (S 2 -S 4 ). Stimulatorul nervului aferent Stoller (SANS) a fost introdus pentru a stimula PTN folosind un electrod de calibru 34 introdus în aceeași locație și utilizat în electroacupunctură (așa-numitul punct SP6), cu un electrod de suprafață plasat în spatele maleolei mediale. [ 6] . În prezent, un dispozitiv comercial (Urgent-PC, Uroplastie, Inc., Minnetonka, Statele Unite ale Americii) folosește această tehnică. De obicei, se utilizează 12 sesiuni de stimulare percutanată a nervului tibial posterior (PTNS), la intervale săptămânale, iar un studiu amplu, randomizat, controlat cu placebo, a arătat o îmbunătățire semnificativă a simptomelor generale de oboseală hiperactivă (60/110) comparativ cu tratamentul simulat (23/110). [7] . S-a demonstrat că pacienții cu răspuns la PTNS pot continua să beneficieze de terapie după 12 luni. [8] . Mecanismul exact al PTNS rămâne neclar și sunt necesare studii multidisciplinare suplimentare pentru a clarifica acest lucru.
În scopul acestei analize, vom lua în considerare doar tehnicile neinvazive, definite ca „o procedură care nu implică introducerea unui instrument în corp”. În plus, definim și stimularea electrică nervoasă transcutanată (TENS) ca o tehnică în care stimulii electrici sunt transmiși prin pielea intactă.
Principalul motiv pentru a ne concentra pe această modalitate este acela că are o serie de avantaje practice în modul în care este pusă în aplicare. Metoda este complet neinvazivă, cu electrozi de suprafață conectați la un stimulator ieftin, alimentat cu baterii, și aplicați pe o zonă adecvată a corpului. Stimulatoarele sunt ușor de utilizat, iar electrozii și bateriile ieftine, de obicei pe bază de hidrogel, reprezintă singurul cost al tratamentului continuu. Tratamentul TENS în sine nu ar trebui să necesite vizite regulate ale pacientului la clinici și se administrează de obicei singur acasă, ceea ce este convenabil pentru pacient. În general, există puține sau deloc efecte secundare ale electrozilor tens, deși uneori pot apărea roșeață sau iritații ale pielii în jurul electrozilor, care dispar odată ce sesiunea de stimulare se încheie. TENS a fost, de asemenea, utilizat timp de câteva decenii pentru controlul durerii. Utilizarea TENS în tratamentul obezității hiperactive și al bolilor tractului urinar inferior este mai puțin bine stabilită.
- Figura 2.
Poziția electrodului pentru stimularea transcutanată a nervului tibial posterior (TPTNS). Stimularea poate fi administrată folosind un aparat convențional de stimulare electrică transcutanată a nervilor (TENS).
Alte tehnici de stimulare electrică minim invazivă, cum ar fi: dopuri, stimulare vaginală anală [9] Şi [10] ; stimulare percutanată (acul este introdus în apropierea unui nerv vizat); sau dispozitivele de stimulare implantate nu fac obiectul acestei analize [4] Şi [5] . În special, dopurile sunt adesea respinse de pacient din cauza jenei și a unui sentiment de impuritate. [11] .
Nervul genital dorsal a fost utilizat ca un alt loc de stimulare [10] folosind electrozi de suprafață pentru a furniza stimuli. Totuși, deoarece această analiză se concentrează pe tehnici convenabile pentru pacienți, nu am examinat aceste studii în detaliu.
2. Metode
Am căutat în baza de date electronică PubMed de la început până în decembrie 2013. Termenii de căutare utilizați au fost „incontinență de urgență”, „urgență”, „vezică hiperactivă”, „incontinență urinară” sau „instabilitate detrusoriană” în combinație cu „stimulare electrică”, „TENS”, „TENS”, „stimulare nervoasă”, „neuromodulare de suprafață”, „stimulare noninvazivă”, „studiu” sau „studiu”. În plus, am urmărit citările din referințele primare ale articolelor relevante pe care baza de date nu le-a putut localiza. Criteriile de excludere au fost: studii care nu erau în limba engleză; studii privind tratamentul incontinenței fecale; cele care implică copii, cele care studiază modele animale; cele care implică stimulare electrică percutanată, stimulare anală, stimulare vaginală/peniană sau dispozitive implantate sau cele care nu s-au concentrat în principal pe simptomele de stocare. O schemă logică a procesului de selecție este prezentată în Fig. 1.
Figura 1.
Diagrama de flux a procesului de selecție a lucrărilor.
Opțiuni de figuri
3. Rezultate
Căutarea primară a identificat 410 articole. Folosind criteriile de excludere definite, am examinat în detaliu 16 articole. Nu am analizat în mod specific studii axate major pe cistită interstițială sau disfuncție biliară, deși acestea sunt menționate acolo unde este cazul.
3.1. stimularea sacrală
În 1996, Hasan și colab. [12] respect S. 3 neuromodulare folosind dispozitive TENS implantate aplicate în regiunea perianală (S 2 -S 3 dermatoame). O îmbunătățire la peste 50% dintre pacienții cu detrusor idiopatic a sugerat potențialul utilizării TENS la nivelul sacralului.
Într-un studiu realizat de Walsh și colab. [13] 1 săptămână de stimulare continuă timp de 12 ore pe zi la S 3 dermatoamele au îmbunătățit semnificativ atât frecvența, cât și nicturia. Cu toate acestea, doar 3/32 de pacienți au continuat terapia și doar intermitent, pe o perioadă maximă de 6 luni de urmărire. Autorii nu au evaluat dacă pacienții au considerat că TENS în ziua 12 a fost inconfortabilă și dacă ar putea duce la întreruperea terapiei.
În urma acestui studiu, un grup de 33 de pacienți cu hiperactivitate a detrusorului și simptome de obstrucție a vezicii hiperactive (OAB), evaluat urodinamic, a raportat efecte similare în cazul stimulării autoadministrate la nivelul zonei sacrale de două ori pe zi, comparativ cu oxibutinina, într-un studiu crossover de 14 săptămâni (6 săptămâni de stimulare + 2 săptămâni de eliminare + 6 săptămâni de stimulare). [14] . Grupul de stimulare a raportat, de asemenea, semnificativ mai puține efecte secundare în comparație cu oxibutinina. Autorii nu au documentat în mod specific un anumit grad de dificultate în aplicarea stimulării la 30% dintre pacienți. Acest lucru poate reflecta inconvenientul aranjamentului electrozilor pe S 2 -S 3 dermatoame sau durata sesiunii zilnice de tratament (până la 6 ore).
Un grup eterogen de pacienți neurogeni cu simptome urinare a fost studiat într-un studiu nerandomizat utilizând un aparat TENS cu electrozi plasați peste fisura natală de două ori pe zi, la domiciliu. [15] . Nouăsprezece din 44 de pacienți au ales să rămână pe aparat după acest studiu, ceea ce este în concordanță cu amploarea efectului benefic raportat al tratamentului.
Un alt studiu de mică amploare, efectuat pe 18 pacienți (7 vezică neurogenă, 5 vezică hiperactivă, 6 nicturie), a raportat o îmbunătățire la 10/18 după 1 lună de stimulare a foramenului sacral posterior. [11] . Autorii au sugerat că acest tip de terapie provoacă mai puțin disconfort decât stimularea vaginală sau anală cu dop. Totuși, contrazicând această afirmație, aceștia au raportat că, în unele cazuri, intensitatea nu a fost setată suficient de mare pentru a produce efecte semnificative la toți pacienții.
3.2. Stimularea nervului tibial posterior (PTNS)
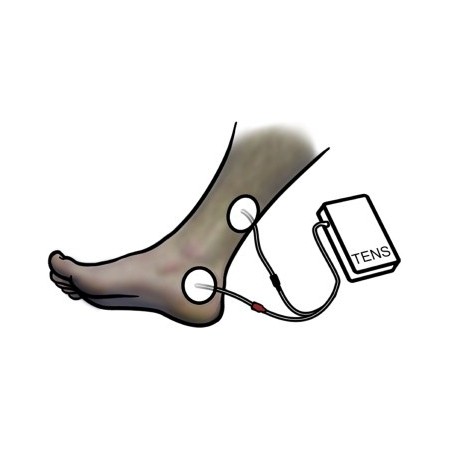
McGuire și colab. [16] a folosit mai întâi stimularea electrică periferică pentru a stimula PTN. În acest studiu inițial, un electrod anodal a fost plasat peste nervul peronier comun sau PTN, iar un electrod catodic a fost plasat peste locul echivalent contralateral. Aceștia au raportat rezultate pozitive la 8/11 pacienți cu hiperactivitate a detrusorului care au devenit uscați după tratament și la șapte pacienți cu boli neurologice (scleroză multiplă, leziuni ale măduvei spinării), dintre care cinci au devenit uscați sau au suferit de o ameliorare a simptomelor. În urma acestui fapt, SANS și, ulterior, dispozitivul Urgent PC au stabilit o bază substanțială de dovezi utilizând abordarea percutanată pentru stimularea PTN, deși într-o locație diferită față de descrierea originală McGuire și colab. a fost folosit. Studii ulterioare privind stimularea nervului tibial posterior (TPTNS), atât percutanată, cât și transcutanată, au utilizat electrozi plasați pe aceeași zonă ca și SANS (Fig. 2). [6] . Prin urmare, TPTNS ar putea fi o opțiune terapeutică plauzibilă și potențial atractivă, bazată pe dovezile disponibile pentru eficacitatea sa în formă percutanată.
Figura 2.
Poziția electrodului pentru stimularea transcutanată a nervului tibial posterior (TPTNS). Stimularea poate fi administrată folosind un aparat convențional de stimulare electrică transcutanată a nervilor (TENS).
Opțiuni de figuri
Eficacitatea personală a TPTNS și oxibutininei comparativ cu grupul de control a fost studiată la 28 de femei cu oboseală hiperactivă. [17] . S-a descris că TPTNS ameliorează simptomele subiective fără evenimente adverse, însă ar fi necesare instrumente de evaluare mai robuste și o documentare atentă a etiopatologiei pacienților studiați pentru a trage concluzii mai detaliate.
A fost raportată o îmbunătățire semnificativă la femeile în vârstă cu incontinență urinară de urgență după 12 săptămâni (o dată pe săptămână) de stimulare în combinație cu exerciții Kegel și antrenament al vezicii urinare. [18] . Totuși, acest efect nu a fost mai mare decât la pacienții dintr-un grup care nu a primit nicio stimulare.
Într-un studiu TPTNS nerandomizat autoadministrat, 83% dintre pacienții cu scleroză multiplă (SM) au raportat ameliorare clinică în departamentul de urgență. [19] . Acest studiu a confirmat, de asemenea, o bună acceptare a terapiei de către pacienți în mediul lor de acasă.
Într-un studiu controlat cu placebo, 37 de femei cu simptome de veac hiperactiv idiopatică au fost randomizate într-un grup de tratament sau unul simulat, cu electrozi plasați în aceeași locație pentru ambele grupuri. [20] . Frecvența urinară s-a îmbunătățit semnificativ, atât în grupul de tratament ( p. = 0,002) și în grupul simulat ( p. = 0,025). Nu s-a obținut o diferență statistic semnificativă între grupuri, un posibil factor de confuzie fiind frecvența inegală a urinării la momentul inițial (13,88 față de 11,35 pe zi).
3.3. Alte locuri de stimulare electrică
Una dintre primele tehnici pentru tratamentul disfuncției de stocare a tractului urinar inferior a stimulat regiunea suprapubiană la pacienții cu sindrom de vezică urinară dureroasă [21] Şi [22] . Această metodă a fost utilizată pentru ameliorarea durerilor abdominale, similar principiului TENS atunci când este utilizată, se presupune, pentru ameliorarea durerii. Frecvență Ulterior, acești pacienți au prezentat și o scădere a frecvenței urinare [22] . Două studii ulterioare au documentat îmbunătățirea parametrilor urodinamici la pacienții cu hiperactivitate detrusoriană (DO), urgență senzorială sau probleme neurogene. Cu toate acestea, pe baza literaturii de specialitate, eficacitatea stimulării locului suprapubian la pacienții cu simptome de veac hiperactiv nu este demonstrată. [23] Şi [24] .
O altă abordare raportată a utilizat stimularea mușchilor coapsei la pacienții cu leziuni ale măduvei spinării pentru ameliorarea spasticii. În unele dintre aceste cazuri, acest lucru a dus la îmbunătățiri ale incontinenței urinare de urgență. [25] și o creștere a capacității cistometrice maxime (MCC) și o reducere a presiunii maxime detrusoriene (MDP) [26] Şi [27] . În plus, 6/19 pacienți au raportat o ameliorare clinică a incontinenței urinare, iar frecvența s-a prelungit timp de 3 luni după tratament. [26] .
Pe baza acestui fapt, în cel mai bun caz, dovezi limitate privind stimularea în alte locuri, cea mai logică abordare utilizată în tehnicile de stimulare electrică transcutanată pare a fi un stimul sacral sau PTNS, deoarece acestea sunt abordate direct sau indirect, S 3 rădăcina măduvei spinării.
3.4. Au aceste efecte de stimulare acută semnificație clinică?
O abordare evidentă pentru a răspunde la această întrebare ar fi evaluarea eficacității stimulării electrice în suprimarea hiperactivității detrusorului (DO), aleasă deoarece se prezintă la mulți pacienți cu simptome de OAB. [28] . Acest lucru i-a determinat pe cercetători să studieze efectele acute ale stimulării electrice în timpul unui studiu urodinamic.
O sută patruzeci și șase de pacienți cu instabilitate detrusoriană idiopatică (IDI), urgență senzorială sau DO secundară bolilor neurogene au prezentat îmbunătățiri ale MCC ( p. = 0,0009) comparativ cu grupul de control (fără stimulare) când stimularea a fost aplicată în timpul S 3 dermatoame [ 29] . În mod similar, Hasan și colab. [12] stimulare comparativ cu același loc, cu simularea și grupurile de control. Cu toate acestea, compararea stimulării suprapubiene, sacrale și simulate realizată de Bower și colab. [23] nu au demonstrat clar aceste efecte imediate asupra MCC. Autorii au concluzionat că îmbunătățirea observată a primei dorințe de a urina (FDV) la pacienți ar putea să nu fie importantă din punct de vedere funcțional, deși o reducere semnificativă a presiunii maxime detrusorului ar putea sugera o potențială eficacitate în DO. O altă abordare a utilizat stimularea condiționată pentru a suprima contracțiile vezicii urinare la 12 pacienți cu scleroză multiplă și hiperactivitate neurogenă a detrusorului (NDO) la nivelul unui loc sacral. [30] și la opt pacienți cu scleroză multiplă (SM) de la PTN [31] folosind un electrod cu ac. Din păcate, niciunul dintre acești pacienți nu a avut un răspuns pozitiv la stimularea dorsală a peniei, unde 10/12 pacienți au reușit să suprime contracția detrusorului. [30] . Nervul dorsal al penisului este o diviziune a nervului pudendal, iar efecte similare ale stimulării electrice au fost demonstrate la stimularea nervului pudendal în alte studii pe oameni. [32] Şi [33] și în modelele animale de pisică [34] Şi [35] . Acest nerv este un nerv profund în regiunea pelviană. Deși s-a sugerat că ar putea fi vizată folosind electrozi de suprafață și o formă de undă de stimulare specifică[34] Şi [35] am reușit să demonstrăm avantajele acestei forme de undă față de o formă de undă de stimulare convențională [36] . Deci se pare că acest nerv poate fi vizat în prezent doar cu electrozi implantați sau electrozi cu ac.
În mod similar, efecte inconsistente se aplică și studiilor privind TPTNS acută, deși Amarenco și colab. [37] a raportat rezultate pozitive la jumătate dintre pacienții cu boli neurologice studiați (scleroză multiplă, leziuni medulare, boala Parkinson). Acești pacienți au prezentat o îmbunătățire cu 50% a volumului la prima contracție a detrusorului și/sau un carcinom multicentric (MCC) de peste 50% față de valoarea inițială. Un studiu urodinamic anterior nu a arătat diferențe semnificative în niciunul dintre parametrii urodinamici la 36 de pacienți cu hiperactivitate a detrusorului. [12] . Acest rezultat diferit s-ar putea datora unor patologii diferite observate la pacienți.
Nicio abordare de identificare a efectelor acute, fie la nivel stimulativ, fie la nivel terapeutic, nu a demonstrat clar și ferm eficacitatea. Cu toate acestea, restul literaturii de specialitate indică faptul că pacienții pot beneficia de efectele neuromodulatoare care pot rezulta din sesiuni repetate de stimulare, mai degrabă decât dintr-o singură aplicare. În plus, de Seze și colab. [19] s-a concluzionat că tratamentul poate fi eficient chiar și la pacienții care nu au răspuns la o TTNS acută inițială aplicată în timpul testării urodinamice.
4. Discuție
4.1. Ce parametri de stimulare?
Literatura de specialitate privind parametrii de stimulare utilizați este rezumată în Tabelul 1, Tabelul 2 și Tabelul 3. Amplasarea electrozilor și gama parametrilor de stimulare sunt probabil factori critici în toate formele de stimulare. Parametrii relevanți ai stimulului includ lățimea impulsului; rata de repetiție a impulsurilor; lungimea exploziei (dacă este cazul) și intensitatea stimulului (de preferință exprimată ca curent, deoarece stimularea prin tensiune, cuplată cu o impedanță incertă a interfeței electrod-țesut, duce la incertitudine cu privire la intensitatea stimulului furnizat). Descrierea tehnică a stimulilor utilizați în unele studii nu oferă toate aceste detalii.
Tabelul 1.
Literatura de specialitate analizează efectele clinice și urodinamice ale TENS în timpul aplicării pe termen lung.
Referinţă | Diagnostic / Caracteristicile pacientului | n. | Loc | parametrii impulsului Stimul | Plan de tratament | Îmbunătățire clinică (% dintre pacienți) | evaluare urodinamică | ||
Frecvenţă | Durata impulsului | Intensitate | |||||||
McGuire și colab. 1983 [16] | MS, SCI, instabilitate detrusoriană, IC | 22 | PTN / nerv peronier comun | - | - | - | - | 80% au devenit uscate sau s-au ameliorat după tratament | - |
Hasan și colab., 1996 [12] | O VREAU | 59 | S. 2 -S 3dermatoame, perianale | 50 Hz | 200 ms | senzație de gâdilare | 2-4 săptămâni, 2 grupuri | Incontinență de urgență 69%, enurezis 73%, frecvență urinară 37% (toate definite ca beneficiu de 50%) | MCC. volumul anulat, n. contracții instabile îmbunătățite semnificativ |
Okada și colab., 1998 [26] | DH, IDI | 19 | regiunea coapsei | 30 Hz, model | 200 ms | Max. sub durere | 2 săptămâni, 1/zi, 20 min | 32% în incontinența urinară și frecvența urinară | Creșterea numărului de pacienți cu MCC în 11/19 ani cu peste 50% |
Walsh și colab., 1999 [13] | IVD refractar | 32 | S. 3dermatoame | 10Hz | 200 ms | - | 1 săptămână, 1 zi, zi 12 ha | 76% în frecvență, 56% reducere a nicturiei, urgenței. Scorul simptomelor pe VAS nu s-a îmbunătățit semnificativ. | - |
Skeil și colab., 2001 [15] | Neurologic | 34 | dermatoame sacrale | 20 Hz | 200 ms | nivel confortabil | 6 săptămâni, 2/zi, 90 min | Îmbunătățire semnificativă a episoadelor de incontinență și a frecvenței acestora | Nu s-a schimbat semnificativ |
Soomro și colab., 2001 [14] | IDI | 43 | S. 3dermatoame | 20 Hz | 200 ms | senzație de gâdilare | 6 săptămâni / până la 360 de minute de traversare zilnică | 56% îmbunătățire cu peste 25% a numărului de goliri zilnice | Nu s-a modificat semnificativ față de grupul de studiu cu stimulare |
Svihra și colab., 2002 [17] | OAB | 28 | PTN | 1Hz | 100 ms | 70% răspuns motor | 5 secunde, 1/săptămână, 30 de minute, 3 grupuri, control | 56% din chestionare au punctaj, grupul de control nu a prezentat niciun semn de diferență. | - |
Yokozuka și colab., 2004 [11] | Vezică neurogenă, instabilă, nicturie | 18 | Sacral S 2-S 4dermatoame | 20 Hz 10s pornit 5s oprit | 300 ms | Controlul sfincterului anal. | 4 săptămâni, 2/zi, 15 min | Îmbunătățire cu 55% a UUI și a frecvenței | Creșterea cu 44% a MCC și inhibarea contracției |
Bellette și colab., 2009 [20] | OAB non-neurogenă, femei | 37 | PTN | - | - | - | 8 s, 2 / săptămână, grup simulat | Frecvența și urgența s-au îmbunătățit semnificativ în ambele grupuri | - |
Schreiner și colab., 2010 [18] | UUI, bătrânele | 51 | PTN | 10Hz | 200 ms | Un anumit răspuns motor | 12 s, 1/săptămână, 30 min, control | UUI s-a îmbunătățit semnificativ cu 76% față de 26,9% dintre pacienții din grupul de control | - |
din Seze și colab. 2011 [19] | DOMNIȘOARĂ | 70 | PTN | 10Hz | 200 ms | Răspuns motor sub așteptări | 3 m, 1 / zi, 20 min | Îmbunătățire cu 83,3% a urgenței în funcție de timp, subscala de urgență MHU și frecvența avertizărilor | fără total. dintre pacienții cu hiperactivitate a detrusorului (86%) a scăzut semnificativ la 73% |
Booth și colab. 2013 [45] | Disfuncție erectilă a vezicii urinare / intestinului, vârstnici | 30 | PTN | 10Hz | 200 ms | nivel de confort | 12 secunde, 2/săptămână, 30 de minute, grup simulat | Frecvență: 74% față de 42% în fals | - |
DH, hiperreflexie detrusoriană; CI, cistită interstițială; IDI, instabilitate detrusoriană idiopatică; IDO, hiperactivitate idiopatică a detrusorului; DIV, disfuncție urinară iritativă; MCC, capacitate cistometrică maximă; MHU, Mesure du Handicap urinaire; scleroză multiplă, scleroză multiplă; OAB, vezică hiperactivă; PTN, nerv tibial posterior; SCI, leziune a măduvei spinării; UP, urgență senzorială; UUI, incontinență urinară de urgență.
Opțiuni tabel
Tabelul 2.
Literatură de specialitate care analizează efectele urodinamice acute ale TENS.
Autor în primul an | Diagnostic | n. | Loc | parametrii impulsului Stimul | detaliile studiului | Rezultatul urodinamicii | ||
Frecvenţă | Lățimea impulsului | Intensitate | ||||||
Hasan și colab., 1996 [12] | IDI | 36 | PTN suprapubian | 50 Hz | 200 ms | senzație de gâdilare | Parte a studiului amplu | Nicio diferență semnificativă în niciunul dintre parametri |
59 | S. 2 -S 3 T. 12Control (fals) | 50 Hz | 200 ms | senzație de gâdilare | 3 grupuri, ficțiune, control | MCC a crescut semnificativ în S 2 -S 3 stimulare vs. simulare și control | ||
Bower și colab., 1998 [23] | DIN, PE | 79 | sacral | 10Hz | 200 ms | Max. senzație tolerabilă | 3 grupuri, simulare | creștere maximă DP și FDV |
suprapubian | 150 Hz | 200 ms | creștere maximă DP și FDV | |||||
ficţiune | niciun stimul | creștere a MCC la punctele Su. | ||||||
Walsh și colab., 2001 [29] | IDI, SU, DH (SCI, MS) | 146 | dermatoame perianale | 10Hz | 200 ms | - | Grupul de control | FDV ( p. = 0,002) și MCC ( p. = 0,0009) s-a îmbunătățit comparativ cu grupul de control |
Amarenco și colab., 2003 [37] | MS, SCI, PD, IDI | 44 | PTN | 10Hz | 200 ms | Răspuns motor sub așteptări | efect acut | Creștere de 48% (21/44) a volumului la FIDC, creștere de 34% (15/44) la MCC |
Fjorback și colab., 2007 [30] | DOMNIȘOARĂ | 12 | sacral | 20 Hz | 500 ms | 50-60mA | stimulare condiționată | 0/12 au reușit să suprime contracția detrusorului |
DPN | 20 Hz | 500 ms | 50-60mA | 10/12 au reușit să suprime contracția detrusorului | ||||
DH, hiperreflexie detrusoriană; DI, instabilitate detrusoriană; DPN, nerv penian/clitoridian dorsal; FDV, prima dorință de a urina; FIDC, prima contracție involuntară a mușchiului detrusor; IDI, instabilitate detrusoriană idiopatică; MCC, capacitate cistometrică maximă; scleroză multiplă, scleroză multiplă; PD, boala Parkinson; PTN, nerv tibial posterior; SCI, leziune a măduvei spinării; UP, urgență senzorială.
Opțiuni tabel
Tabelul 3.
Rezumatul studiilor analizate în funcție de tipul și locul stimulării.
nu dețin controlul | control placebo | O altă formă de control | |
sacral | Yokozuka și colab. [11] | Bower și colab. [23] | Fjorback și colab. [30] |
PTNS | Amarenco și colab. [37] | Booth și colab. [45] | Schreiner și colab. [18] |
Suprapubian / altul | Okada și colab. [26] | Bower și colab. [23] | Hasan și colab. [12] |
Opțiuni tabel
Pentru a obține stimularea sacrală, Yokozuka și colab. [11] Pacienților li s-a recomandat să plaseze electrozi de suprafață peste foramenul sacral posterior și să crească intensitatea stimulării până când se poate simți o contracție anală. Ei au emis ipoteza că, în cazurile în care nu a existat nicio îmbunătățire, electrozii nu au fost plasați în poziția corectă sau intensitatea nu a fost suficient de mare din cauza disconfortului asociat. Există sprijin pentru Takahashi și Tanaka [38] în care modificări ușoare ale poziției electrodului au produs modificări aparente semnificative ale răspunsului la presiunea uretrală [11] . Studiile de stimulare sacrală raportate până în prezent au de obicei electrozi plasați în foramenele sacrale sau pe fese care acoperă S. 2 și S. 3dermatoame. Plasarea precisă a electrozilor pe zonele sacrale variază între studii, probabil pentru că locația dermatomelor sacrale este incertă. [39] Şi [40] . Intensitatea curentului de stimulare a fost de obicei setată la un maxim dictat de pragul durerii. În alte studii, pacienții au fost instruiți să seteze o intensitate care producea o senzație de gâdilare. [12] , [14] Şi [15] . Trunchiurile nervoase (rădăcinile) din aceste zone se află adânc în foramine și este puțin probabil ca acestea să fi fost stimulate direct la nivelul de intensitate a stimulului utilizat. Cu toate acestea, nervii cutanați din dermatomi sunt ușor de stimulat și, prin urmare, stimularea superficială a fibrelor senzoriale, care poate duce atât la modularea directă, cât și indirectă a mecanismelor reflexe ale măduvei spinării, ar putea explica efectele raportate. În plus, intensitatea care produce contracția sfincterului anal [11] Implică stimularea nervilor motori, activând astfel diferite mecanisme și poate provoca de fapt un disconfort semnificativ pacienților. Clarificarea locului exact de stimulare și a intensității necesare trebuie abordate în lucrările viitoare. Pe baza dovezilor disponibile, nu putem concluziona care sunt cei mai buni parametri de stimulare de utilizat pentru stimularea sacrală. Descrierea originală a PTNS de către McGuire și colab. [16] nu s-a repetat în ceea ce privește poziția electrodului. Majoritatea studiilor plasează electrozii în apropierea maleolei mediale, unde netezurul posttraumatic este relativ superficial. Nu este clar pe ce picior trebuie plasați electrozii pentru un răspuns optim și dacă acest lucru contează; unii autori au plasat electrozi pe piciorul stâng [17] , [20] Şi [37] , în timp ce alții pe piciorul drept [18] , [19] Şi [31] . De asemenea, ar putea fi mai eficientă plasarea electrozilor bilateral, deși niciun studiu nu a examinat încă acest lucru. În descrierea setării intensității curente, unele dintre studii au prezentat răspunsuri motorii în timpul stimulării [17] Şi [18] . În alte studii, intensitatea stimulării a fost setată chiar sub pragul motor. [37] sau puțin peste pragul de percepție [19] .
Studiul care raportează cele mai promițătoare rezultate terapeutice este cel realizat de de Seze și colab. [19] , care au raportat tratament PTNS cu succes pentru simptomele OAB la pacienții cu scleroză multiplă. Intensitatea stimulării în acest studiu a fost stabilită sub pragul de percepție, iar pacienții nu au raportat niciun răspuns motor după stimulare. Astfel, doar fibrele senzoriale sau nervii cutanați care acoperă nevralgia posttraumatică au fost probabil stimulați, ceea ce sugerează că acest lucru ar putea fi suficient pentru tratamentul obstrucției aortice hiperactive. Dacă tratamentul este autoadministrat, este probabil ca pacientul să prefere niveluri de stimulare mai scăzute, ceea ce poate duce apoi la stimularea doar a nervilor cutanați, mai degrabă decât a nervului tibial posterior în sine.
4.2. Metodologia de stimulare simulată
Căutarea posibilelor efecte placebo este probabil esențială în studiul noilor terapii, iar acest lucru este valabil în special în cazul tehnicilor de stimulare electrică, datorită senzațiilor pe care le provoacă. Totuși, din cauza acestor senzații, producerea unei stimulări electrice simulate poate fi dificilă. O metodologie simulată interesantă a fost utilizată într-un studiu efectuat pe copii cu oboseală hiperactivă, unde, într-unul dintre ramurile studiului, stimularea a fost aplicată peste scapulă, unde era de așteptat să apară efecte asupra controlului tractului urinar inferior. [41] . În mod similar, Hasan și colab. [12] TENS aplicat deasupra T 12 dermatom care a acționat ca placebo.
Stimularea electrică sub nivelurile pragului motor provoacă senzații de furnicături datorită stimulării structurilor nervoase senzoriale cutanate. O opțiune alternativă pentru o metodologie simulată ar putea fi scăderea treptată a intensității stimulării la zero după câteva secunde de utilizare și indicarea subiectului că stimulii senzaționali se pot estompa în timp. Aceasta este o abordare utilizată pe scară largă în tehnici precum stimularea transcraniană cu curent. [42] . În plus, subiectul se poate adapta la astfel de stimuli încât nu mai este capabil să recunoască dacă stimularea persistă sau nu. Această obișnuință depinde probabil de frecvența stimulării utilizate, de intensitatea stimulilor aplicați și de răspunsurile subiective personale.
O altă abordare în investigarea efectului placebo ar putea fi aplicarea de electrozi pe aceeași zonă a pielii, dar fără curent de stimulare, folosind stimulatoare modificate în acest scop. [43] . Totuși, aceasta presupune că pacientul trebuie să fie naiv la stimularea electrică și, prin urmare, să nu fie conștient de faptul că aceasta provoacă senzație.
Leroi și colab. [44] a efectuat un studiu randomizat, controlat cu simulare, în care pacienților nu li s-a spus că pot primi stimulare simulată. Pacienții au fost randomizați în grupuri cu stimul activ și cu stimul simulat. Această metodologie a fost aprobată de comitetul lor local de etică, deși editorii revistei în care au publicat ulterior lucrările au descurajat puternic cercetătorii suplimentari să utilizeze o astfel de metodologie, deoarece considerau că ar putea reprezenta o încălcare a Declarației de la Helsinki. Considerăm că aceasta este o abordare justificabilă pentru a depăși problemele tehnice legate de supunerea la stimuli fictivi în etapa de aprobare de către comitetul de etică corespunzător. Totuși, trebuie luat în considerare beneficiul pentru pacient al unui astfel de aranjament, iar oferta unui tratament activ, după ce studiul ar putea aborda această problemă.
5. concluzie
Alegerea parametrilor de stimulare, locația aplicării stimulării, măsurile de evaluare a rezultatelor utilizate, precum și afecțiunile și simptomele subiacente studiate au variat foarte mult în literatura de specialitate de până în prezent. Există puține date publicate în literatura de specialitate privind urmărirea pe termen lung și, prin urmare, regimul de tratament care produce beneficii continue este neclar.
Consensul actual este că cel mai promițător loc pentru stimulare este S 3 zona măduvei spinării din regiunea sacrală sau deasupra nervului tibial posterior, dar nu este clar care abordare de administrare a stimulilor este cea mai eficientă. Se cunosc puține lucruri despre mecanismele de acțiune care stau la baza acestora și despre structurile exacte care trebuie stimulate.
Cu toate acestea, există dovezi convingătoare pentru eficacitatea abordării stimulării transcutanate, deși sunt necesare studii suplimentare de amploare, controlate cu placebo, pentru a oferi o bază solidă de dovezi. Standardizarea metodologiei de proces viitoare este importantă pentru a permite comparații între studii și protocoale de stimulare.
- Alimentare: 2 baterii alcaline AA (LR6) de 1,5V;
- Ieșire: 100mApp în sarcină de 1000 Ohm (cu impulsuri de 200mS)
- Lățime impuls: De la 50mS la 400mS reglabilă în trepte de 50mS
- Frecvență: 1Hz până la 150Hz (1-2-3-4-5-10-12-14-16-18-20-25-30-35-40-45-50-60-70-80-90-100-110-120-130-140-150).
- Formă de undă: Impulsuri bifazice simetrice - Impulsuri bifazice alternante.
- Cronometru tratament: Continuu, 10min, 20min, 30min, 45min, 60min, 90min.
- Timpi ACȚIUNE/PAUZĂ: De la 1 la 60 de secunde, reglabili în pași de 1 secundă.
- Timp RAMP: 0 până la 5 secunde, reglabil în pași de 1 secundă.
- Dimensiuni: 138 mm x 6,8 mm x 28 mm.
- Greutate: 160 g. baterii incluse.
- Temperatura de utilizare și depozitare: de la +5 la +35 °C.
- Umiditate relativă pentru utilizare și depozitare: 20% până la 80%.
- Dispozitiv Intellistim BE-28UG
- 2 baterii AA
- cabluri de conectare
- manual de utilizare în italiană
- geantă de călătorie
Sondele trebuie achiziționate separat.
Electrostimulator perineal pentru incontinență Beac IntelliSTIM BE-28UG
- Peste 90.000 de clienți mulțumiți din 2020
- Plăți securizate: card de credit, PayPal și transfer bancar
- Livrare rapidă: Poșta și BRT
- Suport clienți Whatsapp +39 371 43 61 201
Alte produse similare:

Piese de schimb și accesorii:

Cablu NEGRU în Y pentru utilizarea sondelor anal-vaginale cu 4 electrozi și stimulator monocanal

Cablu ROȘU în Y pentru utilizarea sondelor anal-vaginale cu 4 electrozi cu stimulator monocanal

Electrozi din sârmă pentru electrostimulare și TENS 50x50 - 4 buc.

Pereche de cabluri pentru electrostimulatoarele BEAC

PERISPHERA - A - sondă anală cu 4 electrozi
Sondă anală BEAC

Sonda anale Chattanooga Saint-Cloud

Sondă vaginală BEAC Periprobe VAG-2STW
- chevron_left
- 1
- 2
- 3
- 4
- 5
- chevron_right
Aprecierea ta pentru recenzie nu a putut fi trimisa
Reclama un comentariu
Raport trimis
Reclamatia tau nu a putut fi trimisa
Scrie-ti recenzia
Recenzia a fost trimisa
Recenzia ta nu a putut fi trimisa