Elektrostymulator do nietrzymania moczu Beac IntelliSTIM BE-28UG
- Ponad 90 000 zadowolonych klientów od 2020 roku
- Bezpieczne płatności: karta kredytowa, PayPal i przelew bankowy
- Przyspieszona wysyłka: Poste, BRT, FedEx
- Obsługa klienta Whatsapp +39 371 43 61 201
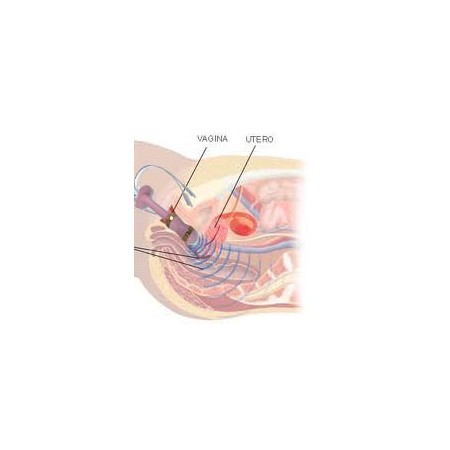
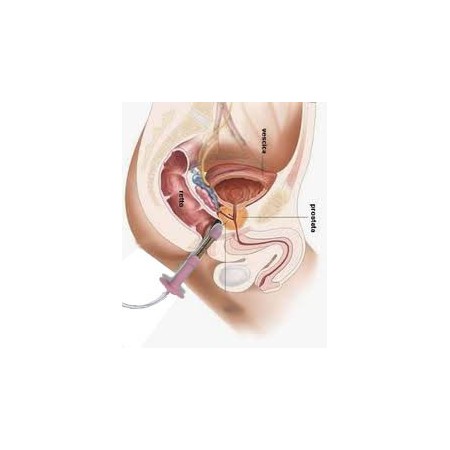
Elektrostymulator krocza BECA 28UG jest urządzeniem terapeutycznym do leczenia nietrzymania moczu za pomocą elektrostymulacji krocza do użytku profesjonalnego lub osobistego.
Intellistim 28UG elektrostymulacja krocza BEAC, przy użyciu sond dopochwowych lub analnych, jest leczeniem z wyboru w wielu przypadkach nietrzymania moczu.
Możliwość uzupełnienia profesjonalnego leczenia o sesje domowe jest często decydująca dla sukcesu terapeutycznego.
Unit IntelliSTIM UG, choć wyposażony w zaawansowane funkcje i elastyczność funkcjonalną wymaganą w zastosowaniach profesjonalnych, jest również łatwy w obsłudze bezpośrednio przez pacjenta.
- Duży wyświetlacz LCD
- Prosta i intuicyjna obsługa
- 4 darmowe programy
- 11 programów do wyboru, odpowiednich do różnych zabiegów na nietrzymanie moczu.
- Funkcja IntelliSTIM z interaktywną automatyczną regulacją parametrów czasowych
- Wyświetlanie wszystkich parametrów i możliwość modyfikacji w trakcie sesji
- 2 kształty fal do wyboru do użytku z sondami pierścieniowymi lub prętowymi.
Urządzenie jest w stanie wykonać stymulację kości piszczelowej w celu leczenia problemów z miednicą poprzez zakup alettrodów.
Nieinwazyjna przezskórna stymulacja elektryczna w leczeniu pęcherza nadreaktywnego
Abstrakt
Dokonaliśmy przeglądu piśmiennictwa na temat przezskórnej elektrycznej stymulacji nerwów (TENS) stosowanej w terapii objawów pęcherza nadreaktywnego (OAB), ze szczególnym uwzględnieniem: miejsca stymulacji, parametrów bodźca, struktur nerwowych uważanych za docelowe oraz uzyskanych wyników klinicznych i urodynamicznych. W większości badań stosowano stymulację nerwu krzyżowego lub piszczelowego. Literatura sugeruje, że chociaż terapia TENS może mieć działanie neuromodulujące, jest mało prawdopodobne, aby pacjent odniósł znaczące korzyści z jednorazowego zastosowania TENS i w rzeczywistości nie zgłoszono oczywistych korzyści z badań ostrych. W badaniach długoterminowych stwierdzono różnice w opisach intensywności stymulacji, strategii terapii i umiejscowienia elektrod, a także w różnych objawach i patologii pacjentów. Ponadto większość badań była niekontrolowana i dlatego nie oceniano efektu placebo. Niewiele wiadomo o podstawowym mechanizmie, za pomocą którego działają te terapie, a zatem o tym, które dokładnie struktury należy stymulować i z jakimi parametrami. Istnieją obiecujące dowody na skuteczność stymulacji przezskórnej, ale potrzebna będzie odpowiednia standaryzacja kryteriów stymulacji i miar wyników, aby określić najlepszy sposób zarządzania tą terapią i udokumentować jej skuteczność.
1. Wprowadzenie
Objawy zespołu pęcherza nadreaktywnego (OAB) to dobrze rozpoznany zestaw objawów, których pacjent doświadcza podczas fazy cyklu oddawania moczu. Charakteryzuje się parciem naglącym (nagłym parciem na mocz, które trudno odłożyć), któremu u prawie wszystkich pacjentów towarzyszy zwiększona częstotliwość i nokturia, a zwłaszcza u pacjentek naglące nietrzymanie moczu [1] . Około jedna trzecia pacjentek cierpi na poważne zaburzenia nietrzymania moczu [2] .
Elektrostymulacja jest stosowana od kilkudziesięciu lat w leczeniu różnych dysfunkcji dolnych dróg moczowych. Stymulator kości krzyżowej Finetech-Bridley ustalił korzeń przedni [3] , wszczepiony elektryczny korzeń krzyżowy (S 2 -S 4 ) stymulator wspomagający opróżnianie pęcherza moczowego, stanowił prekursora dzisiejszych szeroko rozpowszechnionych technik neuromodulacji krzyżowej [4] oraz [5 ] . I S 2 -S 4 Korzenie nerwowe dostarczają moc motoryczną do pęcherza. W szczególności S 3 Korzeń unerwia głównie mięsień wypieracza i jest głównym celem neuromodulacji krzyżowej.
Innym ważnym i dobrze ugruntowanym miejscem stymulacji jest tylny nerw piszczelowy (PTN). PTN jest nerwem mieszanym zawierającym L 5 -S 3 włókna, ponownie pochodzące z tych samych segmentów kręgosłupa, co unerwienie przywspółczulne do pęcherza moczowego (S 2 -S 4 ). Wprowadzono aferentny stymulator nerwu Stollera (SANS) do stymulacji PTN za pomocą elektrody o rozmiarze 34 włożonej w to samo miejsce i stosowanej w elektroakupunkturze (tzw. punkt SP6), z elektrodą powierzchniową umieszczoną za kostką przyśrodkową [ 6] . Obecnie urządzenie komercyjne (Urgent-PC, Uroplastyka, Inc., Minnetonka, USA) wykorzystuje tę technikę. Zwykle stosuje się 12 sesji tylnej przezskórnej stymulacji nerwu piszczelowego (PTNS), w odstępach tygodniowych, a duże randomizowane badanie kontrolowane placebo wykazało znaczną poprawę ogólnych objawów OAB (60/110) w porównaniu z pozorami (23/110) [7] . Wykazano, że pacjenci z PTNS mogą nadal odnosić korzyści z terapii przez ponad 12 miesięcy [8] . Dokładny mechanizm PTNS pozostaje niejasny w badaniach multidyscyplinarnych i potrzebne są dalsze badania, aby to wyjaśnić.
Na potrzeby tego przeglądu rozważymy wyłącznie techniki nieinwazyjne, zdefiniowane jako "procedura, która nie wymaga wprowadzenia narzędzia do organizmu". Ponadto definiujemy również przezskórną elektryczną stymulację nerwów (TENS) jako technikę, w której bodźce elektryczne są przepuszczane przez nieuszkodzoną skórę.
Głównym powodem, dla którego warto skupić się na tym trybie, jest to, że ma on wiele praktycznych zalet w swojej dostawie. Metoda jest całkowicie nieinwazyjna, z elektrodami powierzchniowymi przymocowanymi do taniej baterii stymulatora i aplikowanymi w odpowiednie miejsce na ciele. Stymulatory są łatwe w użyciu dzięki niedrogim, zwykle hydrożelowym elektrodom i bateriom, które są jedynym kosztem trwającego leczenia. Samo leczenie TENS nie powinno wymagać regularnych wizyt pacjenta w przychodniach i zazwyczaj jest wykonywane samodzielnie w domu, co jest wygodne dla pacjenta. Ogólnie rzecz biorąc, dziesiątki nie występują żadne skutki uboczne, chociaż czasami może wystąpić zaczerwienienie lub podrażnienie skóry wokół elektrod, które ustępuje po zakończeniu sesji stymulacji. TENS jest również stosowany od kilkudziesięciu lat do kontroli bólu. Zastosowanie TENS w leczeniu OAB i chorób dolnych dróg moczowych jest mniej ugruntowane.
- Rysunek 2.
Lokalizacja elektrody do przezskórnej tylnej stymulacji nerwu piszczelowego (TPTNS). Stymulacja może być dostarczona za pomocą konwencjonalnego urządzenia do przezskórnej elektrycznej stymulacji nerwów (TENS).
Inne małoinwazyjne techniki stymulacji elektrycznej, takie jak: zatyczki, stymulacja pochwy [9] i [10] ; stymulacja przezskórna (igła jest wprowadzana w pobliżu docelowego nerwu); o wszczepione urządzenia stymulacyjne wykraczają poza zakres niniejszego przeglądu [4] i [5] . W szczególności zatyczki są często odrzucane przez pacjenta z powodu zakłopotania i poczucia nieczystej linii [11] .
Grzbietowy nerw narządów płciowych został wykorzystany jako kolejne miejsce stymulacji [10] Używanie elektrod powierzchniowych do dostarczania bodźców. Ponieważ jednak niniejszy przegląd koncentruje się na technikach dogodnych dla pacjentów, nie dokonaliśmy szczegółowego przeglądu tych badań.
2. Metody
Przeszukaliśmy elektroniczną bazę danych PubMed od początku do grudnia 2013 roku. Wyszukiwane hasła to: "naglące nietrzymanie moczu", "parcie naglące", "pęcherz nadreaktywny", "nietrzymanie moczu" lub "niestabilność wypieracza" w połączeniu ze "stymulacją elektryczną", "tens", "tens", "stymulacja nerwów", "powierzchnia neuromodulacji", "stymulacja nieinwazyjna", "próba" lub "badanie". Ponadto śledziliśmy cytaty z głównych odniesień do odpowiednich artykułów, których baza danych nie mogła zlokalizować. Kryteriami wykluczenia były: badania, które nie były prowadzone w języku angielskim; badania nad leczeniem nietrzymania stolca; te, w których uczestniczą dzieci, te, które badają modele zwierzęce; te, które obejmują przezskórną stymulację elektryczną, stymulację odbytu, stymulację pochwy/prącia lub wszczepione urządzenia lub te, które nie koncentrowały się głównie na objawach spichrzeniowych. Schemat blokowy procesu selekcji przedstawiono na rys. 1.
Rysunek 1.
Schemat blokowy procesu sortowania papieru.
Opcje figur
3. Wyniki
W badaniach pierwotnych zidentyfikowano 410 pozycji. Korzystając ze zdefiniowanych kryteriów wykluczenia, szczegółowo przyjrzeliśmy się 16 artykułom. Nie dokonaliśmy szczegółowego przeglądu badań z większym stężeniem na śródmiąższowym zapaleniu pęcherza moczowego lub zaburzeniach wad, chociaż są one wymienione w stosownych przypadkach.
3.1. Stymulacja sakralna
W 1996 roku Hasan i wsp. [12] Szacunek S 3 neuromodulacja za pomocą wszczepionych urządzeń z TENS aplikowanych na okolicę odbytu (S 2 -S 3 dermomaki). Poprawa u ponad 50% pacjentów z wypieraczami idiopatycznymi sugeruje możliwość zastosowania TENS w miejscu krzyżowym.
W badaniu przeprowadzonym przez Walsha i wsp. [13] 1 tydzień od ciągłej stymulacji przez 12 godzin dziennie w S 3 Dermatomy znacznie poprawiły zarówno częstotliwość, jak i nokturię. Jednak tylko 3/32 pacjentów kontynuowało terapię i to tylko z przerwami, przez okres do 6 miesięcy obserwacji. Autorzy nie ocenili, czy u pacjentów, u których stwierdzono TENS w 12. dniu, było to nieprzyjemne i potencjalnie mogło prowadzić do przerwania leczenia.
Po tym badaniu urodynamicznie oszacowana grupa 33 pacjentów cierpiących na nadpobudliwość wypieracza i objawy OAB zgłosiła podobne efekty w przypadku samodzielnej stymulacji miejsca krzyżowego dwa razy dziennie w porównaniu z oksybutyniną w 14-tygodniowym badaniu krzyżowym (stymulacja 6 w +2 wymywanie w +6 w stymulacji) [14] . Grupa stymulująca zgłosiła również znacznie mniej skutków ubocznych w porównaniu z oksybutyniną. Autorzy nie udokumentowali konkretnie pewnego stopnia trudności w stosowaniu stymulacji u 30% pacjentów. Może to odzwierciedlać niedogodności związane z umieszczaniem elektrod na S 2 -S 3 dermatomów lub długość dziennej sesji zabiegowej (do 6 h).
Heterogeniczna grupa pacjentów neurogennych z objawami ze strony układu moczowego została przebadana w nierandomizowanym badaniu przy użyciu urządzenia TENS z elektrodami umieszczonymi nad szczeliną porodową dwa razy dziennie w warunkach domowych [15] . Dziewiętnastu z 44 pacjentów zdecydowało się zachować maszynę po tym badaniu, zgodnie z zgłoszonym korzystnym efektem leczenia.
W innym małym badaniu z udziałem 18 pacjentów (7 pęcherza neurogennego, 5 OAB, 6 nokturii) odnotowano poprawę u 10/18 po 1 miesiącu stymulacji tylnego otworu krzyżowego [11] . Autorzy zasugerowali, że ten rodzaj terapii powoduje mniejszy dyskomfort niż stymulacja pochwy czy kręgosłupa odbytu. Jednakże, w przeciwieństwie do tego twierdzenia, stwierdzili, że w niektórych przypadkach intensywność nie była ustawiona na wystarczająco wysokim poziomie, aby wywołać znaczące efekty u wszystkich pacjentów.
3.2. Stymulacja tylnego nerwu piszczelowego (PTNS)
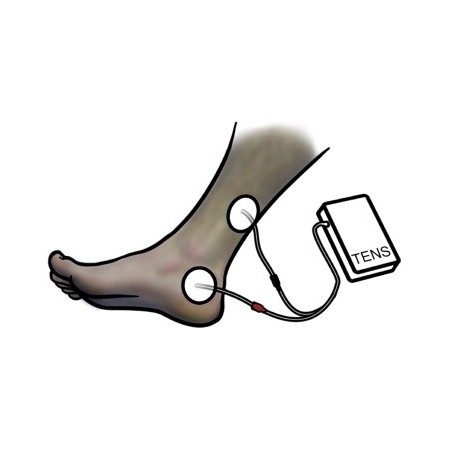
McGuire i wsp. [16] po raz pierwszy zastosowano obwodową stymulację elektryczną w celu stymulacji PTN. W tym wstępnym badaniu elektrodę anodową umieszczono na wspólnym nerwie strzałkowym lub PTN, a elektrodę katodową umieszczono nad przeciwległym miejscem równoważnym. Stwierdzili pozytywne wyniki u pacjentów z nadpobudliwością wypierającą 8/11, u których doszło do wyschnięcia po leczeniu, oraz u siedmiu pacjentów z chorobami neurologicznymi (stwardnienie rozsiane, uszkodzenie rdzenia kręgowego), z których pięciu stało się suchych lub poprawiło się. Następnie SANS, a następnie urządzenie Urgent PC stworzyły istotną bazę dowodową przy użyciu przezskórnego podejścia do stymulacji PTN, chociaż użyto innej lokalizacji niż pierwotny opis McGuire i wsp. W dalszych badaniach przezskórnej lub przezskórnej tylnej stymulacji nerwu piszczelowego (TPTNS) wykorzystano elektrody umieszczone na tym samym obszarze co SANS (ryc. 2) [6] . W związku z tym TPTNS może być wiarygodną i potencjalnie atrakcyjną opcją leczenia w oparciu o dostępne dowody na jej przezskórną skuteczność.
Rysunek 2.
Lokalizacja elektrody do przezskórnej tylnej stymulacji nerwu piszczelowego (TPTNS). Stymulacja może być dostarczona za pomocą konwencjonalnego urządzenia do przezskórnej elektrycznej stymulacji nerwów (TENS).
Opcje figur
Osobistą skuteczność TPTNS i oksybutyniny w porównaniu z grupą kontrolną oceniano u 28 kobiet z OAB [17] . TPTNS został opisany jako poprawiający subiektywne objawy bez zdarzeń niepożądanych, ale do wyciągnięcia bardziej szczegółowych wniosków potrzebne byłyby solidniejsze narzędzia oceny i staranna dokumentacja etiopatologii badanych pacjentów.
U starszych kobiet z naglącym nietrzymaniem moczu odnotowano znaczną poprawę po 12 tygodniach (raz w tygodniu) stymulacji w połączeniu z ćwiczeniami Kegla i tworzeniem pęcherza moczowego [18] . Efekt ten nie był jednak lepszy u pacjentów w grupie, która w ogóle nie otrzymywała bodźca.
W nierandomizowanym badaniu TPTNS do samodzielnego wykonania 83% pacjentów ze stwardnieniem rozsianym (SM) zgłosiło poprawę kliniczną w nagłych wypadkach [19] . Badanie to potwierdziło również dobrą akceptację terapii przez pacjentów w ich środowisku rodzinnym.
W badaniu kontrolnym placebo 37 kobiet z objawami idiopatycznego OAB zostało losowo przydzielonych do grupy leczonej lub pozorowanej z elektrodami umieszczonymi w tym samym miejscu dla obu grup [20] . Znaczna poprawa częstości oddawania moczu, zarówno w grupie leczonej ( p = 0,002) i w grupie pozorowanej ( p = 0,025). Nie osiągnięto statystycznie istotnej różnicy między grupami, a możliwym czynnikiem zakłócającym była nierówna wyjściowa częstotliwość oddawania moczu (13,88 Vs. 11.35 dziennie).
3.3. Inne miejsca stymulacji elektrycznej
Jedna z pierwszych technik leczenia dysfunkcji niskomagazynowej stymulowanego odcinka nadłonowego dróg moczowych u pacjentów z zespołem bolesnego pęcherza moczowego [21] i [22] . Ta metoda została zastosowana w celu złagodzenia bólu brzucha, podobnie jak zasada TENS, gdy jest stosowana w celu złagodzenia bólu. Następnie pacjenci ci doświadczyli również zmniejszonego oddawania moczu [22] . Dwa kolejne badania udokumentowały poprawę parametrów urodynamicznych u pacjentów z nadpobudliwością wypieracza (DO), popędami czuciowymi lub problemami neurogennymi. Na podstawie piśmiennictwa nie wykazano jednak skuteczności stymulacji miejsca nadłonowego u pacjentów z objawami OAB [23] i [24] .
W innym opisanym podejściu zastosowano stymulację mięśni ud u pacjentów z uszkodzeniem rdzenia kręgowego w celu złagodzenia spastyczności. W niektórych z tych przypadków doprowadziło to do poprawy w zakresie nagłego nietrzymania moczu [25] oraz zwiększenie maksymalnej pojemności cystometrycznej (MCC) i zmniejszenie maksymalnego ciśnienia wypieracza (MDP) [26] i [27] . Ponadto 6/19 pacjentów zgłosiło kliniczną poprawę w zakresie nietrzymania moczu, a częstość ta utrzymuje się przez 3 miesiące po leczeniu [26] .
Opierając się na tym, w najlepszym razie ograniczonych dowodach na stymulację w innych miejscach, najbardziej logicznym podejściem do zastosowania w technikach przezskórnej stymulacji elektrycznej wydaje się być bodziec krzyżowy lub PTNS, ponieważ są one bezpośrednio lub pośrednio adresowane, S 3 korzeń rdzenia kręgowego.
3.4. Czy ostre efekty stymulujące mają znaczenie kliniczne?
Oczywistym podejściem do odpowiedzi na to pytanie byłaby ocena skuteczności stymulacji elektrycznej w tłumieniu nadpobudliwości wypieracza (DO), wybranej, ponieważ występuje ona u wielu pacjentów z objawami OAB [28] . To skłoniło naukowców do zbadania ostrych skutków stymulacji elektrycznej podczas badania urodynamicznego.
Stu czterdziestu sześciu pacjentów z idiopatyczną niestabilnością wypieracza (IDI), popędami czuciowymi lub DO wtórnymi do chorób neurogennych wykazało poprawę MCC ( p = 0,0009) w porównaniu z grupą kontrolną (bez stymulacji), gdy stymulacja była stosowana w trakcie S 3 dermatomy [ 29] . Podobnie Hasan i wsp. [12] Stymulacja w porównaniu z tym samym miejscem pozorowanym i grupami kontrolnymi. Jednak porównanie stymulacji nadłonowej, krzyżowej i pozorowanej przez Bowera i wsp. [23] nie wykazały wyraźnie tych bezpośrednich skutków dla MCC. Autorzy doszli do wniosku, że zaobserwowana poprawa w zakresie pierwszego głodu pustki (FDV) u pacjentów może nie być funkcjonalnie istotna, chociaż znaczne zmniejszenie maksymalnego ciśnienia wypieracza może sugerować potencjalną skuteczność w DO. W innym podejściu wykorzystano stymulację warunkową w celu stłumienia skurczów pęcherza moczowego u 12 pacjentów ze stwardnieniem rozsianym z nadreaktywnością neurogenną wypieracza (NDO) w miejscu kości krzyżowej [30] oraz u ośmiu pacjentów ze stwardnieniem rozsianym w PTN [31] za pomocą elektrody igłowej. Niestety, żaden z tych pacjentów nie miał pozytywnej odpowiedzi na stymulację grzbietową prącia, w której 10/12 pacjentów było w stanie stłumić skurcz wypieracza [30] . Nerw grzbietowy prącia jest podziałem nerwu sromowego, a podobne efekty stymulacji elektrycznej wykazano podczas stymulacji nerwu sromowego w obu innych badaniach na ludziach [32] i [33] oraz w modelach zwierzęcych kotów [34] i [35] . Ten nerw jest nerwem głęboko w okolicy miednicy. Chociaż zasugerowano, że można go ukierunkować za pomocą elektrod powierzchniowych i specyficznego kształtu fali stymulacyjnej[34] i [35] Byliśmy w stanie zademonstrować zalety tego kształtu fali w porównaniu z konwencjonalnym kształtem fali stymulacyjnej [36] . Wydawałoby się więc, że nerw ten może być celowany tylko za pomocą elektrod igłowych lub obecnie.
Podobnie niespójne efekty dotyczą badań nad ostrym TPTNS, chociaż Amarenco i wsp. [37] stwierdzono pozytywne wyniki u połowy badanych pacjentów z chorobami neurologicznymi (stwardnienie rozsiane, SCI, choroba Parkinsona). U tych pacjentów wykazano 50% poprawę objętości przy pierwszym wypieraczu i (lub) skurczu MCC o ponad 50% wartości wyjściowej. Wcześniejsze badanie urodynamiczne nie wykazało istotnych różnic w żadnym z parametrów urodynamicznych u 36 pacjentów z nadpobudliwością wypieracza [12] . Ten odmienny wynik może być spowodowany różnymi patologiami obserwowanymi u pacjentów.
Żadne z podejść do poszukiwania ostrych efektów, czy to w miejscu stymulującym, nie wykazało wyraźnie i stanowczo skuteczności. Jednak bilans piśmiennictwa wskazuje, że pacjenci mogą odnieść korzyści z efektów neuromodulujących, które mogą wynikać z powtarzających się sesji stymulacji, a nie z jednorazowego zastosowania. Ponadto de Seze i wsp. [19] stwierdzono, że leczenie może być skuteczne nawet u pacjentów, którzy nie zareagowali na początkowy ostry TTNS zastosowany podczas badania urodynamicznego.
4. Dyskusja
4.1. Jakie parametry stymulacji?
Literaturę dotyczącą zastosowanych parametrów stymulacji podsumowano w Tabeli 1, Tabeli 2 i Tabeli 3. Lokalizacja elektrod i zakres parametrów bodźca mogą być czynnikami krytycznymi we wszystkich formach stymulacji. Istotne parametry bodźca obejmują szerokość impulsu; częstotliwość powtarzania impulsów; długość impulsu (jeśli dotyczy) i intensywność bodźca (najlepiej określana jako prąd, ponieważ stymulacja napięciowa w połączeniu z niepewną impedancją interfejsu elektroda-tkanka prowadzi do niepewności co do siły dostarczonego bodźca). Techniczny opis bodźców stosowanych w niektórych badaniach nie podaje wszystkich tych szczegółów.
Tabela 1.
W piśmiennictwie dokonano przeglądu klinicznych i urodynamicznych skutków TENS podczas długotrwałego stosowania.
Odniesienie | Diagnostyka/charakterystyka pacjenta | n | Miejsce | Parametry impulsu Bodziec | Schemat leczenia | Poprawa kliniczna (% pacjentów) | Ocena urodynamiczna | ||
Częstotliwość | Czas trwania impulsu | Intensywność | |||||||
McGuire i in. 1983 [16] | MS, SCI, wyboczenie wyboczeniowe, IC | 22 | PTN / Nerw strzałkowy wspólny | - | - | - | - | 80% wyschło lub poprawiło się po zabiegu | - |
Hasan et al., 1996 [12] | TAK | 59 | S 2 -S 3dermatomy okołoodbytnicze | 50 Hz | Czas trwania: 200 ms | uczucie łaskotania | 2-4 W, 2 grupy | naglące nietrzymanie moczu 69%, moczenie nocne 73%, częstość oddawania moczu 37% (wszystkie zdefiniowane jako 50% korzyści) | MCC. objętość anulowana, brak skurczów niestabilnych znacznie się poprawił |
Okada et al., 1998 [26] | DH, UID | 19 | Okolice ud | 30 Hz, model | Czas trwania: 200 ms | Max. pod wpływem bólu | 2 W, 1/gł., 20 min | 32% w przypadku nietrzymania moczu i częstość jego występowania | Wzrost liczby pacjentów z MCC u 11/19 wynosi ponad 50% |
Walsh et al., 1999 [13] | Ogniotrwałe diagnostyka in vitro | 32 | S 3dermatomy | 10 Hz | Czas trwania: 200 ms | - | 1 W, 1/D, Dzień 12 ha | 76% częstość, 56% zmniejszenie nokturii, parcie naglące Ocena objawów w VAS nie uległa znaczącej poprawie | - |
Skeil et al., 2001 [15] | Neurologiczny | 34 | Deratomy krzyżowe | 20 Hz | Czas trwania: 200 ms | Komfortowy poziom | 6 W, 2 / dzień, 90 min | Znaczna poprawa w epizodach i częstości występowania nietrzymania moczu | Nie zmienił się znacząco |
Soomro i wsp., 2001 [14] | IDE | 43 | S 3dermatomy | 20 Hz | Czas trwania: 200 ms | uczucie łaskotania | 6 W / Do 360 min dziennego czasu przesuwu | O 56% poprawiono o ponad 25% liczbę dziennych pustostanów | Nie zmieniło się zauważalnie w porównaniu z ramieniem badawczym stymulacji |
Svihra et al., 2002 [17] | OAB | 28 | PTN | 1 Hz | Czas trwania: 100 ms | 70% odpowiedzi silnika | 5 s, 1/W, 30 min, 3 grupy, sterowanie | 56% wyników kwestionariuszy, grupa kontrolna bez znaku różnicy. | - |
Yokozuka et al., 2004 [11] | Neurogenny, niestabilny pęcherz, nokturia | 18 | Sakralny S 2-S 4dermatomy | 20 Hz od 10 s do 5 s wył. | Czas trwania: 300 ms | Zwieracz odbytu. | 4 W, 2 / dzień, 15 min | O 55% poprawiony UUI i częstotliwość | O 44% zwiększano MCC i hamowano skurcze |
Bellette et al., 2009 [20] | Nieneurogenny OAB, kobiety | 37 | PTN | - | - | - | 8 S, 2/W, Grupa pozorna | Częstość i pilność uległy znacznej poprawie w obu grupach | - |
Schreiner i in., 2010 [18] | UUI, kobiety w podeszłym wieku | 51 | PTN | 10 Hz | Czas trwania: 200 ms | Pewna reakcja motoryczna | 12 s, 1/W, 30 min, sterowanie | UUI znacznie się poprawiło w 76% Vs 26,9% pacjentów w grupie kontrolnej | - |
de Seze i in. 2011 [19] | TĘSKNIĆ | 70 | PTN | 10 Hz | Czas trwania: 200 ms | Niedostateczna reakcja silnika | 3 m, 1 / dzień, 20 min | 83,3% poprawiło pilność w oparciu o czas, pilność podskali MHU i częstotliwość ostrzeżeń | Brak sumy. pacjentów nadpobudliwość wypieracza (86%) istotnie zmniejszyła się do 73% |
Booth i in. 2013 [45] | Pęcherz / Jelita erekcyjne, Osoby w podeszłym wieku | 30 | PTN | 10 Hz | Czas trwania: 200 ms | Poziom komfortu | 12 s, 2/w, 30 min, Grupa pozorna | Częstotliwość: 74% Vs. 42% w podróbce | - |
DH, hiperrefleksyjny detruzator; IC, śródmiąższowe zapalenie pęcherza moczowego; IDI, idiopatyczna niestabilność wypieracza; IDO, idiopatyczna nadpobudliwość wypieracza; IVD, zaburzenia podrażnień i opróżniania; MCC, maksymalna pojemność cystometrii; MHU, pisuar dla niepełnosprawnych; SM, stwardnienie rozsiane; OAB, pęcherz nadreaktywny; PTN, tylny nerw piszczelowy; SCI, uraz rdzenia kręgowego; SU, parcie na zmysły; UUI, naglące nietrzymanie moczu.
Opcje tabel
Tabela 2.
Przegląd piśmiennictwa dotyczący ostrych urodynamicznych skutków TENS.
Pierwszy rok autorstwa | Diagnoza | n | Miejsce | Parametry impulsu Bodziec | Szczegóły badania | Wynik urodynamiczny | ||
Częstotliwość | Szerokość impulsu | Intensywność | ||||||
Hasan et al., 1996 [12] | IDE | 36 | PTN nadłonowy | 50 Hz | Czas trwania: 200 ms | uczucie łaskotania | Część obszernego badania | Brak znaczącej różnicy w którymkolwiek z parametrów |
59 | S 2 -S 3 T 12(fikcja) Kontrola | 50 Hz | Czas trwania: 200 ms | uczucie łaskotania | 3 Grupy, Fikcja, Kontrola | MCC istotnie zwiększył się w S 2 -S 3 Stymulacja w porównaniu do pozorowania i kontroli | ||
Bower et al., 1998 [23] | Z DNIA | 79 | Sakralna | 10 Hz | Czas trwania: 200 ms | Max. znośne odczucia | 3 grupy, Pozory | wzrost DP i FDV |
nadłonowy | 150 Hz | Czas trwania: 200 ms | wzrost DP i FDV | |||||
fikcja | Brak bodźca | wzrost MCC do Su pts. | ||||||
Walsh et al., 2001 [29] | IDI, SU, DH (NARTY, MS) | 146 | Dermatomy okołoodbytnicze | 10 Hz | Czas trwania: 200 ms | - | Grupa kontrolna | FDV ( p = 0,002) i MCC ( p = 0,0009) jest lepszy w porównaniu z kontrolą |
Amarenco et al., 2003 [37] | MS, SCI, PD, IDI | 44 | PTN | 10 Hz | Czas trwania: 200 ms | Niedostateczna reakcja silnika | Efekt ostry | 48% (21/44) wzrost wolumenu w FIDC, 34% (15/44) wzrost MCC |
Fjorback et al., 2007 [30] | TĘSKNIĆ | 12 | Sakralna | 20 Hz | Czas trwania: 500 ms | 50-60 mA | Stymulacja warunkowa | 0/12 było w stanie stłumić skurcz wypieracza |
DPN | 20 Hz | Czas trwania: 500 ms | 50-60 mA | 10/12 było w stanie stłumić skurcz wypieracza | ||||
DH, hiperrefleksyjny detruzator; DI, wyboczenie wyboczeniowe; DPN, grzbietowy prącie/nerw łechtaczkowy; FDV, pierwsze pragnienie oddania moczu; FIDC, pierwszy mimowolny skurcz mięśnia wypieracza; IDI, idiopatyczna niestabilność wypieracza; MCC, maksymalna pojemność cystometrii; SM, stwardnienie rozsiane; PD, choroba Parkinsona; PTN, tylny nerw piszczelowy; SCI, uraz rdzenia kręgowego; SU, parcie na zmysły.
Opcje tabel
Tabela 3.
Podsumowanie badań dokonanych w zależności od rodzaju i miejsca stymulacji.
Brak kontroli | Kontrola placebo | Inne formy kontroli | |
Sakralna | Yokozuka i wsp. [11] | Bower i wsp. [23] | Fjorback i wsp. [30] |
PTNS | Amarenco i wsp. [37] | Booth i wsp. [45] | Schreiner i wsp. [18] |
Nadłonowy / inny | Okada i wsp. [26] | Bower i wsp. [23] | Hasan i wsp. [12] |
Opcje tabel
Aby osiągnąć stymulację krzyżową, Yokozuka i wsp. [11] Pacjenci, których zadaniem było umieszczenie elektrod powierzchniowych na tylnym otworze krzyżowym i zwiększenie intensywności stymulacji do skurczu odbytu, mogli być odczuwalni. Postawili hipotezę, że w przypadkach, w których nie było poprawy, elektrody nie były umieszczane we właściwej pozycji lub intensywność nie była wystarczająco wysoka ze względu na związany z tym dyskomfort. Jest wsparcie dla Takahashiego i Tanaki [38] w którym niewielkie zmiany w położeniu elektrod powodowały zauważalne zmiany w reakcji na ciśnienie w cewce moczowej [11] . W dotychczas zgłoszonych badaniach stymulacji krzyżowej zwykle umieszcza się elektrody w otworach krzyżowych lub na pośladkach leżących nad literą S 2 oraz S 3dermomy. Dokładne rozmieszczenie elektrod w świętych miejscach różni się w zależności od badania, prawdopodobnie dlatego, że lokalizacja dermatomów krzyżowych jest niepewna [39] i [40] . Natężenie prądu stymulacyjnego było zwykle ustawione na maksimum podyktowane progiem bólu. W innych badaniach pacjenci zostali poinstruowani, aby ustawić intensywność, która wywoływała uczucie łaskotania [12] , [14] i [15] . Pnie nerwowe (korzenie) w tych obszarach znajdują się głęboko w otworach i jest mało prawdopodobne, aby były one bezpośrednio stymulowane na poziomie intensywności używanego bodźca. Jednak nerwy skórne w dermatomach są łatwe do stymulacji, a zatem powierzchowna stymulacja włókien czuciowych, która może prowadzić zarówno do bezpośredniej, jak i pośredniej modulacji mechanizmów odruchu rdzenia kręgowego, może wyjaśniać zgłaszane efekty. Ponadto intensywność, która powoduje skurcz zwieracza odbytu [11] Polega na stymulacji nerwów ruchowych, aktywując w ten sposób różne mechanizmy, a nawet może powodować znaczny dyskomfort u pacjentów. Wyjaśnienie dokładnego miejsca stymulacji i wymaganej intensywności powinno zostać uwzględnione w przyszłych pracach. Na podstawie dostępnych danych naukowych nie jesteśmy w stanie stwierdzić, jakie parametry stymulacji najlepiej stosować do stymulacji krzyżowej. Oryginalny opis PTNS autorstwa McGuire'a i wsp. [16] Nie powtórzyło się to pod względem położenia elektrod. Większość badań umieszcza elektrody w pobliżu kostki przyśrodkowej, gdzie PTN jest stosunkowo płytki. Nie jest jasne, na której nodze należy umieścić elektrody, aby uzyskać optymalną reakcję i czy jest to ważne; Niektórzy autorzy umieścili elektrody na lewej nodze [17] , [20] i [37] , podczas gdy inni na prawej nodze [18] , [19] i [31] . Może być również bardziej skuteczny w przypadku umieszczania elektrod dwustronnie, chociaż nie zbadano jeszcze tego w żadnych badaniach. Opisując aktualne ustawienie intensywności, niektóre z badań przedstawiały reakcje motoryczne podczas stymulacji [17] i [18] . W innych badaniach intensywność stymulacji została ustawiona na nieco poniżej progu motorycznego [37] lub tuż powyżej progu percepcji [19] .
Badanie, w którym przedstawiono najbardziej obiecujące wyniki terapeutyczne, zostało przeprowadzone przez de Seze i wsp. [19] , w którym odnotowano sukces PTNS w leczeniu objawów OAB u pacjentów ze stwardnieniem rozsianym. Intensywność stymulacji w tym badaniu została ustawiona powyżej progu percepcji, a pacjenci nie zgłaszali żadnych reakcji motorycznych po stymulacji. Tak więc tylko włókna czuciowe lub nerwy skórne pokrywające PTN były prawdopodobnie stymulowane, co sugeruje, że może to być wystarczające do leczenia OAB. Jeśli leczenie jest podawane samodzielnie, jest prawdopodobne, że pacjent wolałby niższe poziomy stymulacji, co może prowadzić do stymulacji samych nerwów skórnych, a nie samego tylnego nerwu piszczelowego.
4.2. Metodologia stymulacji pozorowanej
Badania nad możliwymi efektami placebo są prawdopodobnie niezbędne w badaniach nad nowymi terapiami, a dotyczy to zwłaszcza technik stymulacji elektrycznej ze względu na odczucia, jakie wywołują. Jednak ze względu na te odczucia wytwarzanie pozorowanej stymulacji elektrycznej może być trudne. Ciekawą metodologię przeprowadzono w badaniu dzieci z OAB, gdzie w jednym ramieniu badania zastosowano stymulację nad łopatką, gdzie spodziewano się wpływu na kontrolę dolnych dróg moczowych [41] . Podobnie Hasan i wsp. [12] TENS zastosowany na T 12 dermatom, który działał jak placebo.
Stymulacja elektryczna poniżej progu motorycznego powoduje uczucie mrowienia z powodu stymulacji struktur nerwów czuciowych skóry. Alternatywną opcją dla metodologii pozorowanej może być stopniowe zmniejszanie intensywności stymulacji do zera po kilku sekundach użytkowania i wskazanie badanemu, że bodźce doznaniowe mogą z czasem zanikać. Jest to podejście szeroko stosowane w technikach takich jak przezczaszkowa stymulacja prądem [42] . Ponadto badany może przystosować się do takich bodźców, że tak naprawdę nie jest w stanie rozpoznać, czy stymulacja utrzymuje się, czy nie. To przyzwyczajenie może zależeć od częstotliwości stosowanej stymulacji, siły zastosowanych bodźców i osobistych subiektywnych reakcji.
Innym podejściem w badaniach nad efektem placebo może być przyłożenie elektrod do tego samego obszaru skóry, ale bez prądu stymulacyjnego przy użyciu zmodyfikowanych do tego celu stymulatorów [43] . Zakłada to jednak, że pacjent musi być naiwny co do stymulacji elektrycznej, a zatem nie wiedzieć, że powoduje ona odczucia.
Leroi i wsp. [44] Przeprowadzono randomizowane badanie kontrolne pozorowane, w którym pacjentom nie powiedziano, że mogą otrzymać stymulację pozorowaną. Pacjenci zostali losowo przydzieleni do grup bodźców aktywnych i pozorowanych. Metodologia ta została zatwierdzona przez lokalną komisję etyczną, chociaż redaktorzy czasopisma, w którym są one następnie publikowane, zdecydowanie odradzają badaczom stosowanie takiej metodologii, ponieważ uważają, że może ona stanowić naruszenie Deklaracji Helsińskiej. Uważamy, że jest to uzasadnione podejście do przezwyciężenia problemów technicznych fikcyjnych bodźców poddanych mu na etapie zatwierdzania przez odpowiednią komisję etyczną. Należy jednak wziąć pod uwagę korzyści dla pacjenta wynikające z takiego rozwiązania, a oferta aktywnego leczenia po badaniu mogłaby rozwiązać ten problem.
5. Wnioski
Dobór parametrów stymulacji, lokalizacja zastosowanej stymulacji, zastosowane miary wyników oraz podstawowe schorzenia i objawy badane są bardzo różne w dotychczasowej literaturze. W piśmiennictwie opublikowano niewiele danych dotyczących obserwacji długoterminowej, dlatego nie jest jasne, jaki schemat leczenia przyniesie trwałe korzyści.
Obecny konsensus jest taki, że najbardziej obiecującym miejscem stymulacji jest S 3 obszar rdzenia kręgowego w okolicy krzyżowej lub powyżej tylnego nerwu piszczelowego, ale nie jest jasne, które podejście do dostarczania bodźców jest najskuteczniejsze. Niewiele wiadomo na temat mechanizmów leżących u podstaw działania i tego, że należy stymulować dokładne struktury.
Istnieją jednak kuszące dowody na skuteczność metody stymulacji przezskórnej, chociaż potrzebne są dalsze duże badania kontrolowane placebo, aby zapewnić solidną bazę wiedzy. Standaryzacja przyszłej metodologii procesów jest ważna, aby umożliwić dokonywanie porównań między badaniami a protokołami stymulacji.
Specyfikacje:
- Zasilanie: 2 baterie alkaliczne 1,5 V AA (LR6);
- Wyjście: 100 mApp przy obciążeniu 1000 Ohm (z impulsami 200mS)
- Szerokość impulsu: od 50 mS do 400 mS regulowana w krokach co 50 mS
- Częstotliwość: od 1 Hz do 150 Hz (1-2-3-4-5-10-12-14-16-18-20-25-30-35-40-45-50-60-70-80-90-100-110-120-130-140-150).
- Kształt fali: symetryczne impulsy dwufazowe - zmienne impulsy dwufazowe.
- Timer zabiegu: ciągły, 10 min, 20 min, 30 min, 45 min, 60 min, 90 min.
- Czasy AKCJI/PAUZY: od 1 do 60 s, regulowane w krokach od 1 sek.
- Czas RAMP: od 0 do 5 sekund, regulowany w krokach od 1 sekundy.
- Wymiary: 138mm x 6 8mm x 28mm.
- Waga: 160 g. baterie w zestawie.
- Temperatura pracy i przechowywania: od +5 do +35 °C.
- Wilgotność względna użytkowania i przechowywania: od 20% do 80%.
Sprzęt:
- Urządzenie Intellistim BE-28UG
- 2 baterie rysika
- połączeniowe
- instrukcja obsługi w języku angielskim
- Walizka podróżna
Sondy należy zakupić osobno.
Elektrostymulator do nietrzymania moczu Beac IntelliSTIM BE-28UG
- Ponad 90 000 zadowolonych klientów od 2020 roku
- Bezpieczne płatności: karta kredytowa, PayPal i przelew bankowy
- Szybka wysyłka: poczta i BRT
- Obsługa klienta Whatsapp +39 371 43 61 201
Inne podobne produkty:

Części zamienne i akcesoria:

CZERWONY Y do użytku 4-elektrodowe sondy analne - dopochwowe ze stymulatorem jednokanałowym

Drut elektrodowy do elektrostymulacji i tensów 50x50 - 4 szt.

Para do elektrostymulatorów BEAC

PERISPHERA - A - 4-elektrodowa sonda analna
Sonda analna BEAC

Sonda analna Chattanooga Saint-Cloud

Sonda dopochwowa BEAC Periprobe-2STW
Sonda dopochwowa BEAC Perisphera - O z 2 elektrodami
- chevron_left
- 1
- 2
- 3
- 4
- 5
- chevron_right
Chwilowo nie możesz polubić tej opinii
Zgłoś komentarz
Zgłoszenie wysłane
Twoje zgłoszenie nie może zostać wysłane
Napisz swoją opinię
Recenzja została wysłana
Twoja recenzja nie może być wysłana