Perineale incontinentie elektrostimulator Beac IntelliSTIM BE-28UG
- Meer dan 90.000 tevreden klanten sinds 2020
- Veilige betalingen: creditcard, PayPal en bankoverschrijving
- Versnelde verzending: Poste, BRT, FedEx
- Klantenservice Whatsapp +39 371 43 61 201
De BECA 28UG perineale elektrostimulator is een therapeutische eenheid voor de behandeling van incontinentie, door middel van perineale elektrostimulatie, voor professioneel of persoonlijk gebruik.
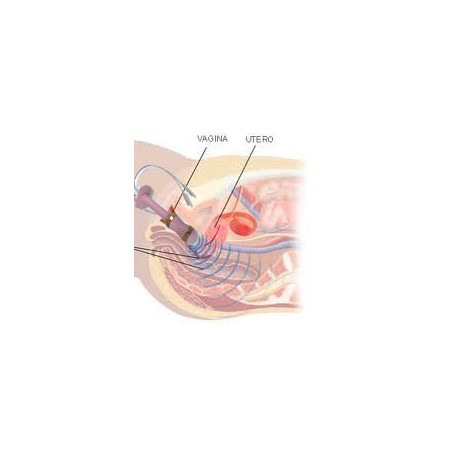
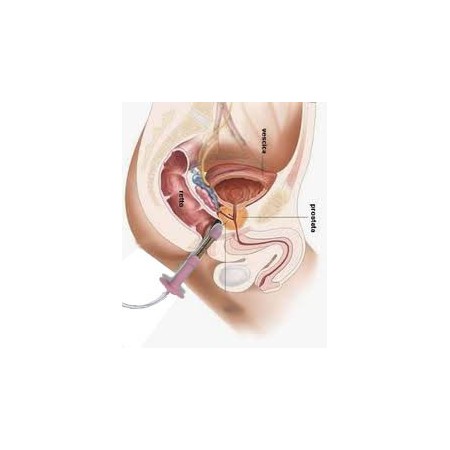
BEAC's Intellistim 28UG perineale elektrostimulatie, met behulp van vaginale of anale sondes, is de voorkeursbehandeling in veel gevallen van urine-incontinentie.
De mogelijkheid om een professionele behandeling aan te vullen met thuissessies is vaak doorslaggevend voor therapeutisch succes.
De IntelliSTIM UG-unit is weliswaar uitgerust met geavanceerde functies en functionele flexibiliteit die vereist zijn voor professioneel gebruik, maar is ook gemakkelijk direct door de patiënt te gebruiken.
- Groot LCD-scherm
- Eenvoudig en intuïtief te gebruiken
- 4 gratis programma's
- 11 selecteerbare programma's, geschikt voor verschillende incontinentiebehandelingen.
- IntelliSTIM-functie met interactieve automatische aanpassing van tijdparameters
- Weergave van alle parameters en mogelijkheid tot wijziging tijdens de sessie
- 2 selecteerbare golfvormen voor gebruik met ring- of staafsondes.
Het apparaat is in staat om tibiale stimulatie uit te voeren voor de behandeling van bekkenproblemen door de alettrodes aan te schaffen.
Niet-invasieve transcutane elektrische stimulatie bij de behandeling van een overactieve blaas
Abstract
We hebben de literatuur over transcutane elektrische zenuwstimulatie (TENS) beoordeeld die wordt gebruikt als therapie voor symptomen van een overactieve blaas (OAB), met bijzondere aandacht voor: stimulatieplaats, stimulusparameters, neurale structuren waarvan wordt aangenomen dat ze het doelwit zijn, en bereikte klinische en urodynamische resultaten. De meeste onderzoeken hebben sacrale of tibiale zenuwstimulatie gebruikt. De literatuur suggereert dat, hoewel TENS-therapie neuromodulerende effecten kan hebben, het onwaarschijnlijk is dat de patiënt significant baat zal hebben bij een enkele toepassing van TENS en dat er in feite geen duidelijke voordelen van acute studies zijn gerapporteerd. In langetermijnstudies waren er verschillen in beschrijvingen van stimulatie-intensiteit, therapiestrategie en plaatsing van de elektroden, evenals in de verschillende symptomen en pathologie van de patiënten. Bovendien waren de meeste onderzoeken ongecontroleerd en evalueerden daarom het placebo-effect niet. Er is weinig bekend over het basismechanisme waarmee deze therapieën werken en dus precies welke structuren moeten worden gestimuleerd, en met welke parameters. Er is veelbelovend bewijs voor de werkzaamheid van een transcutane stimulatiebenadering, maar adequate standaardisatie van stimulatiecriteria en uitkomstmaten zal nodig zijn om de beste manier te bepalen om deze therapie te beheren en de werkzaamheid ervan te documenteren.
1. Inleiding
Symptomen van het overactieve blaassyndroom (OAB) zijn een algemeen erkende reeks symptomen die de patiënt ervaart tijdens de plascyclusfase. Het wordt gekenmerkt door urgentie (een plotselinge aandrang om te plassen die moeilijk uit te stellen is) die bij bijna alle patiënten gepaard gaat met verhoogde frequentie en nycturie en, vooral bij vrouwelijke patiënten, met aandrangincontinentie [1] . Ongeveer een derde van de vrouwelijke patiënten wordt ernstig gestoord door urine-incontinentie [2] .
Elektrische stimulatie wordt al tientallen jaren gebruikt bij de behandeling van verschillende disfuncties van de lagere urinewegen. De Finetech-Bridley Sacraal Stimulator heeft de voorste wortel vastgesteld [3] , een geïmplanteerde elektrische sacrale wortels (S 2 -S 4 ) stimulator om te helpen bij het legen van de blaas, vormde een voorloper van de huidige wijdverbreide sacrale neuromodulatietechnieken [4] en [5 ] . I S 2 -S 4 Zenuwwortels leveren het motorische principe kracht aan de blaas. Met name de S 3 De wortel innerveert voornamelijk de detrusorspier en is het belangrijkste doelwit van sacrale neuromodulatie.
Een andere belangrijke en gevestigde plaats van stimulatie is die van de achterste scheenbeenzenuw (PTN). De PTN is een gemengde zenuw die L bevat 5 -S 3 vezels, die weer afkomstig zijn van dezelfde spinale segmenten als de parasympathische innervaties naar de blaas (S 2 -S 4 ). De afferente Stoller-zenuwstimulator (SANS) werd geïntroduceerd om PTN te stimuleren met behulp van een 34-gauge elektrode die op dezelfde plaats wordt ingebracht en wordt gebruikt bij elektro-acupunctuur (het zogenaamde SP6-punt), met een oppervlakte-elektrode die achter de mediale malleolus wordt geplaatst [ 6] . Momenteel maakt een commercieel apparaat (Urgent-PC, Uroplasty, Inc., Minnetonka, VS) gebruik van deze techniek. Gewoonlijk worden 12 sessies van posterieure percutane, tibiale zenuwstimulatie (PTNS), met wekelijkse tussenpozen, gebruikt en een grote gerandomiseerde, placebogecontroleerde studie toonde een significante verbetering van de algehele OAB-symptomen (60/110) in vergelijking met schijnvertoningen (23/110) [7] . Het is aangetoond dat PTNS-responders langer dan 12 maanden baat kunnen blijven hebben bij therapie [8] . Het exacte mechanisme van PTNS blijft onduidelijk, multidisciplinaire studies en verdere studies zijn nodig om dit op te helderen.
Voor de doeleinden van deze review gaan we alleen niet-invasieve technieken beschouwen, gedefinieerd als "een procedure waarbij geen instrument in het lichaam wordt ingebracht". Daarnaast definiëren we transcutane elektrische zenuwstimulatie (TENS) ook als een techniek waarbij elektrische prikkels door intacte huid worden geleid.
De belangrijkste reden om op deze modus te focussen, is dat deze een aantal praktische voordelen heeft bij de levering. De methode is volledig niet-invasief, met oppervlakte-elektroden die zijn bevestigd aan een goedkope stimulatorbatterij en op een geschikte plaats op het lichaam worden aangebracht. Stimulatoren zijn gemakkelijk te gebruiken met de goedkope, meestal op hydrogel gebaseerde, elektroden en batterijen die de enige kosten zijn van de lopende behandeling. TENS-behandeling zelf zou geen regelmatige bezoeken van de patiënt aan klinieken moeten vereisen en wordt meestal zelf thuis toegediend, wat handig is voor de patiënt. Over het algemeen zijn er tientallen tot geen bijwerkingen, hoewel er soms roodheid of irritatie van de huid rond de elektroden kan optreden die verdwijnt zodra de stimulatiesessie voorbij is. TENS wordt ook al tientallen jaren gebruikt voor pijnbestrijding. Het gebruik van TENS bij de behandeling van OAB en aandoeningen van de lagere urinewegen is minder ingeburgerd.
- Figuur 2.
Elektrodelocatie voor transcutane posterieure tibiale zenuwstimulatie (TPTNS). Stimulatie kan worden toegediend met behulp van een conventionele transcutane elektrische zenuwstimulatie (TENS) machine.
Andere minimaal invasieve elektrostimulatietechnieken zoals: pluggen, vaginale anale stimulatie [9] en [10] ; percutane stimulatie (naald wordt in de buurt van een gerichte zenuw ingebracht); o Geïmplanteerde stimulatieapparaten vallen buiten het bestek van deze recensie [4] en [5] . Met name de pluggen worden vaak door de patiënt afgewezen vanwege schaamte en een gevoel van onreinheid [11] .
De dorsale genitale zenuw werd gebruikt als een andere plaats van stimulatie [10] oppervlakte-elektroden gebruiken om stimuli te geven. Aangezien deze review zich echter richt op technieken die handig zijn voor patiënten, hebben we deze onderzoeken niet in detail beoordeeld.
2. Methoden
We hebben de elektronische database van PubMed doorzocht vanaf het begin tot december 2013. De gebruikte zoektermen waren 'aandrangincontinentie', 'urgentie', 'overactieve blaas', 'urine-incontinentie' of 'detrusorinstabiliteit' in combinatie met 'elektrische stimulatie', 'tientallen', 'tientallen', 'zenuwstimulatie', 'neuromodulatieoppervlak', 'niet-invasieve stimulatie', 'proef' of 'studie'. Daarnaast volgden we citaties uit primaire verwijzingen naar relevante artikelen die de database niet kon vinden. Uitsluitingscriteria waren: studies die niet in het Engels waren; onderzoeken naar de behandeling van fecale incontinentie; die waarbij kinderen betrokken zijn, die diermodellen bestuderen; die waarbij sprake is van percutane elektrische stimulatie, anale stimulatie, vaginale/penisstimulatie of geïmplanteerde apparaten of die niet primair gericht waren op opslagsymptomen. Een stroomschema van het selectieproces is weergegeven in Fig. 1.
Figuur 1.
Stroomschema van het papiersorteerproces.
Afbeelding opties
3. Resultaten
Primair onderzoek identificeerde 410 items. Aan de hand van de gedefinieerde uitsluitingscriteria hebben we 16 artikelen in detail bekeken. We hebben niet specifiek studies beoordeeld met een hogere concentratie op interstitiële cystitis of ongeldige disfunctie, hoewel deze waar nodig worden vermeld.
3.1. Sacrale stimulatie
In 1996 hebben Hasan et al. [12] Respect S 3 neuromodulatie met behulp van geïmplanteerde apparaten met TENS toegepast op het perianale gebied (S 2 -S 3 dermomen). Verbetering bij meer dan 50% van de idiopathische patiënten met detrusor suggereerde het potentieel van het gebruik van TENS op een sacrale plaats.
In een studie van Walsh et al. [13] 1 week vanaf continue stimulatie gedurende 12 uur per dag bij S 3 Dermatomen verbeterden zowel de frequentie als de nycturie aanzienlijk. Slechts 3 van de 32 patiënten gingen echter door met de therapie, en alleen met tussenpozen, gedurende maximaal 6 maanden follow-up. De auteurs beoordeelden niet of patiënten die TENS voor dag 12 hadden, het ongemakkelijk hadden en mogelijk konden leiden tot stopzetting van de therapie.
Na deze studie rapporteerde een urodynamisch geschatte groep van 33 patiënten die leden aan detrusorhyperactiviteit en OAB-symptomen vergelijkbare effecten voor zelftoegediende stimulatie over de sacrale plaats tweemaal daags in vergelijking met oxybutynine in een 14 weken durende cross-over studie (6 w stimulatie +2 wash-out w +6 w stimulatie) [14] . De stimulatiegroep rapporteerde ook veel minder bijwerkingen in een oxybutyninevergelijking. De auteurs documenteerden niet specifiek een bepaalde moeilijkheidsgraad bij het toepassen van stimulatie bij 30% van de patiënten. Dit kan een weerspiegeling zijn van het ongemak van het plaatsen van elektroden op S 2 -S 3 dermatomen of de duur van de dagelijkse behandelingssessie (tot 6 uur).
Een heterogene groep neurogene patiënten met urinaire symptomen werd bestudeerd in een niet-gerandomiseerde studie met behulp van een TENS-machine met elektroden die tweemaal daags in een thuisomgeving over de natale spleet werden geplaatst [15] . Negentien van de 44 patiënten besloten de machine na deze proef te houden, in overeenstemming met het gerapporteerde gunstige effect van de behandeling.
Een andere kleine studie van 18 patiënten (7 neurogene blaas, 5 OAB, 6 nycturie) rapporteerde een verbetering van 10/18 na 1 maand stimulatie van het achterste sacrale foramen [11] . De auteurs suggereerden dat dit type therapie minder ongemak veroorzaakt dan stimulatie van de vaginale of anale wervelkolom. In tegenstelling tot deze bewering rapporteerden ze echter dat in sommige gevallen de intensiteit niet hoog genoeg was ingesteld om bij alle patiënten significante effecten te hebben.
3.2. Stimulatie van de achterste scheenbeenzenuw (PTNS)
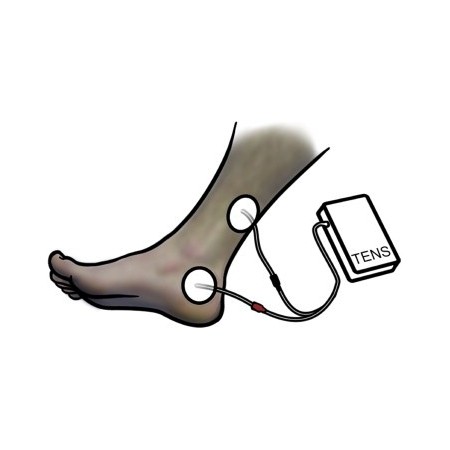
McGuire et al. [16] gebruikte eerst perifere elektrische stimulatie om PTN te stimuleren. In deze eerste studie werd een anode-elektrode op de gemeenschappelijke peroneale zenuw of PTN geplaatst en werd een kathode-elektrode over de contralaterale equivalente plaats geplaatst. Ze rapporteerden positieve resultaten bij 8/11 detrusorhyperactiviteitspatiënten die droog werden na de behandeling, en bij zeven patiënten met neurologische aandoeningen (multiple sclerose, ruggenmergletsel) van wie er vijf droog of verbeterd werden. Hierna hebben de SANS en vervolgens het Urgent PC-apparaat een substantiële bewijsbasis opgebouwd met behulp van de percutane benadering om PTN te stimuleren, hoewel een andere locatie dan de oorspronkelijke beschrijving McGuire et al. werd gebruikt. Verdere studies van percutane of transcutane posterieure tibiale zenuwstimulatie (TPTNS) gebruikten elektroden die op hetzelfde gebied als de SANS werden geplaatst (Fig. 2) [6] . Daarom zou TPTNS een plausibele en potentieel aantrekkelijke behandelingsoptie kunnen zijn op basis van het beschikbare bewijs voor de percutane werkzaamheid ervan.
Figuur 2.
Elektrodelocatie voor transcutane posterieure tibiale zenuwstimulatie (TPTNS). Stimulatie kan worden toegediend met behulp van een conventionele transcutane elektrische zenuwstimulatie (TENS) machine.
Afbeelding opties
De persoonlijke werkzaamheid van TPTNS en oxybutynine versus controle werd onderzocht bij 28 vrouwen met OAB [17] . TPTNS is beschreven als het verbeteren van subjectieve symptomen zonder bijwerkingen, maar robuustere beoordelingsinstrumenten en zorgvuldige documentatie van de etiopathologie van de bestudeerde patiënten zouden nodig zijn om meer gedetailleerde conclusies te trekken.
Een significante verbetering bij oudere vrouwen met aandrangincontinentie werd gemeld na 12 weken (eenmaal per week) stimulatie in combinatie met Kegel-oefeningen en blaasvorming [18] . Dit effect was echter niet superieur aan patiënten in een groep die helemaal geen stimulus kregen.
In een zelf toegediende TPTNS niet-gerandomiseerde studie meldde 83% van de patiënten met multiple sclerose (MS) klinische verbetering in noodgevallen [19] . Deze studie bevestigde ook een goede acceptatie van therapie door patiënten in hun gezinsomgeving.
In een placebocontrolestudie werden 37 vrouwen met symptomen van idiopathische OAB gerandomiseerd in een behandelings- of schijngroep met elektroden die voor beide groepen op dezelfde plaats waren geplaatst [20] . Sterk verbeterde urinefrequentie, zowel in de behandelingsgroep ( p = 0,002) en in de Sham-groep ( p = 0,025). Een statistisch significant verschil tussen de groepen werd niet bereikt, een mogelijke verstorende factor was de ongelijke aanvangsfrequentie van het plassen (13,88 Vs. 11,35 per dag).
3.3. Andere plaatsen van elektrische stimulatie
Een van de eerste technieken voor de behandeling van lage stapelingsdisfunctie van het gestimuleerde suprapubische gebied van de urinewegen bij patiënten met pijnlijk blaassyndroom [21] en [22] . Deze methode is gebruikt om buikpijn te verlichten, vergelijkbaar met het principe van TENS wanneer het zogenaamd wordt gebruikt voor pijnverlichting. Vervolgens ervoeren deze patiënten ook verminderde urineweginfecties [22] . Twee daaropvolgende studies documenteerden een verbetering van urodynamische parameters bij patiënten met detrusorhyperactiviteit (DO), sensorische aandrang of neurogene problemen. Op basis van de literatuur is de werkzaamheid van stimulatie van een suprapubische plaats bij patiënten met OAB-symptomen echter niet aangetoond [23] en [24] .
Een andere gerapporteerde benadering heeft gebruik gemaakt van dijspierstimulatie bij patiënten met een dwarslaesie om spasticiteit te verlichten. In sommige van deze gevallen heeft dit geleid tot verbeteringen in aandrangincontinentie [25] en een verhoging van de maximale cystometriecapaciteit (MCC) en een verlaagde maximale detrusordruk (MDP) [26] en [27] . Daarnaast meldden 6/19 patiënten een klinische verbetering van urine-incontinentie, en de frequentie duurt tot 3 maanden na de behandeling [26] .
Op basis van dit, op zijn best beperkt bewijs voor stimulatie op andere plaatsen, lijkt de meest logische benadering die moet worden gebruikt in transcutane elektrische stimulatietechnieken een sacrale stimulus of PTNS te zijn, aangezien deze direct of indirect worden aangepakt, de S 3 wortel van het ruggenmerg.
3.4. Zijn acute stimulerende effecten van klinische betekenis?
Een voor de hand liggende benadering om deze vraag te beantwoorden, zou zijn om de werkzaamheid van elektrische stimulatie te evalueren bij het onderdrukken van detrusorhyperactiviteit (DO), gekozen omdat het zich voordoet bij veel patiënten met OAB-symptomen [28] . Dit bracht de onderzoekers ertoe om de acute effecten van elektrische stimulatie te bestuderen tijdens een urodynamica-onderzoek.
Honderdzesenveertig patiënten met idiopathische detrusorinstabiliteit (IDI), sensorische drang of DO secundair aan neurogene ziekten vertoonden verbeteringen in MCC ( p = 0,0009) vergeleken met controles (zonder stimulatie) wanneer stimulatie werd toegepast in de loop van S 3 dermatomen [ 29] . Zo ook Hasan et al. [12] Stimulatie in vergelijking met dezelfde schijnplaats en controlegroepen. Echter, de vergelijking van suprapubische, sacrale en schijnstimulatie door Bower et al. [23] hebben deze onmiddellijke effecten op MCC niet duidelijk aangetoond. De auteurs concludeerden dat de waargenomen verbetering van first void craving (FDV) bij patiënten mogelijk niet functioneel belangrijk is, hoewel een significante verlaging van de maximale detrusordruk kan wijzen op potentiële werkzaamheid bij DO. Een andere benadering maakte gebruik van voorwaardelijke stimulatie om samentrekkingen van de blaas te onderdrukken bij 12 MS-patiënten met detrusor neurogene overactiviteit (NDO) op een heiligbeenplaats [30] en bij acht MS-patiënten in het PTN [31] met behulp van een naaldelektrode. Helaas had geen van deze patiënten een positieve respons op dorsale penisstimulatie waarbij 10/12 patiënten in staat waren om de contractie van de detrusor te onderdrukken [30] . De dorsale zenuw van de penis is een afdeling van de nervus pudendus, en vergelijkbare effecten van elektrische stimulatie zijn aangetoond bij het stimuleren van de nervus pudendus in beide andere studies bij mensen [32] en [33] en in kattendiermodellen [34] en [35] . Deze zenuw is een zenuw diep in het bekkengebied. Hoewel er is gesuggereerd dat het kan worden gericht met behulp van oppervlakte-elektroden en een specifieke stimulatiegolfvorm[34] en [35] We waren in staat om de voordelen van deze golfvorm ten opzichte van een conventionele stimulatiegolfvorm aan te tonen [36] . Het lijkt er dus op dat deze zenuw alleen kan worden aangevallen met naaldelektroden of op dit moment.
Soortgelijke inconsistente effecten zijn van toepassing op acute TPTNS-studies, hoewel Amarenco et al. [37] rapporteerde positieve resultaten bij de helft van de onderzochte patiënten met neurologische aandoeningen (MS, dwarslaesie, ziekte van Parkinson). Deze patiënten vertoonden een volumeverbetering van 50% bij de eerste contractie van de detrusor en/of MCC van meer dan 50% van de uitgangswaarde. Een eerdere urodynamische studie toonde geen significante verschillen in een van de urodynamische parameters bij 36 patiënten met detrusorhyperactiviteit [12] . Dit andere resultaat kan misschien te wijten zijn aan verschillende pathologieën die bij patiënten zijn waargenomen.
Geen van beide benaderingen voor het zoeken naar acute effecten, of het nu op een stimulerende plaats is, heeft de werkzaamheid duidelijk en onomstotelijk aangetoond. De balans van de literatuur geeft echter aan dat patiënten baat kunnen hebben bij neuromodulerende effecten die het gevolg kunnen zijn van herhaalde stimulatiesessies, in plaats van een enkele toepassing. Daarnaast hebben de Seze et al. [19] concludeerde dat de behandeling effectief kan zijn, zelfs bij patiënten die niet hebben gereageerd op een eerste acute TTNS die tijdens urodynamisch onderzoek is toegepast.
4. Discussie
4.1. Welke stimulatieparameters?
De literatuur over de gebruikte stimulatieparameters is samengevat in tabel 1, tabel 2 en tabel 3. De locatie van de elektroden en het bereik van stimulusparameters zijn waarschijnlijk kritische factoren bij alle vormen van stimulatie. Relevante stimulusparameters zijn onder meer de pulsbreedte; hartslag herhalingssnelheid; Burst-lengte (indien van toepassing) en intensiteit van de stimulus (bij voorkeur aangeduid als stroom als spanningsstimulatie in combinatie met onzekere impedantie-elektrode-weefselinterface leidt tot onzekerheid over de sterkte van de gegeven stimulus). De technische beschrijving van de stimuli die in sommige onderzoeken worden gebruikt, geeft niet al deze details.
Tabel 1.
Literatuuronderzoek naar de klinische en urodynamische effecten van TENS tijdens toepassing op lange termijn.
Referentie | Diagnostiek/patiëntkenmerken | n | Plaats | Impuls Parameters Stimulus | Behandelschema | Klinische verbetering (% patiënten) | Urodynamische evaluatie | ||
Frequentie | Puls duur | Intensiteit | |||||||
McGuire et al. 1983 [16] | MS, SCI, knik detrusor, IC | 22 | PTN / gemeenschappelijke peroneale zenuw | - | - | - | - | 80% werd droog of verbeterd na behandeling | - |
Hasan et al., 1996 [12] | JA | 59 | S 2 -S 3dermatomen, perianaal | 50 Hz | 200 ms | kietelend gevoel | 2-4 W, 2 groepen | urgentie-incontinentie 69%, enuresis 73%, urinaire frequentie 37% (allemaal gedefinieerd als 50% voordeel) | MCC. volume geannuleerd, geen contracties van instabiel significant verbeterd |
Okada et al., 1998 [26] | DH, UID | 19 | Dij Regio | 30 Hz, model | 200 ms | Max. onder pijn | 2 W, 1/D, 20 min | 32% bij urine-incontinentie en frequentie | 11/19 MCC-patiënten nemen toe met meer dan 50% |
Walsh et al., 1999 [13] | Vuurvaste IVD | 32 | S 3dermatomen | 10 Hz | 200 ms | - | 1 W, 1/D, Dag 12 ha | 76% in frequentie, 56% vermindering in nycturie, urgentie Symptoomscore op VAS niet significant verbeterd | - |
Skeil et al., 2001 [15] | Neurologisch | 34 | Sacrale dermatomen | 20 Hz | 200 ms | Comfortabel niveau | 6 W, 2 / dag, 90 min | Aanzienlijke verbetering van incontinentie-episodes en -frequentie | Niet significant veranderd |
Soomro et al., 2001 [14] | IDES | 43 | S 3dermatomen | 20 Hz | 200 ms | kietelend gevoel | 6 met tot 360 min dagelijkse reistijd | 56% verbeterde met meer dan 25% in het aantal dagelijkse urines | Niet merkbaar veranderd ten opzichte van de stimulatieonderzoeksarm |
Svihra et al., 2002 [17] | OAB | 28 | PTN (NL) | 1 Hz | 100 ms | 70% motorische respons | 5 s, 1/w, 30 min, 3 groepen, bediening | 56% van de vragenlijsten scoort, controlegroep geen verschilteken. | - |
Yokozuka et al., 2004 [11] | Neurogene, instabiele blaas, nycturie | 18 | Sacraal S 2-S 4dermatomen | 20 Hz 10 s tot 5 s uit | 300 ms | Anale contr sluitspier. | 4 W, 2 / dag, 15 min | 55% verbeterd in UUI en frequentie | 44% verhoogde MCC en remde contractie |
Bellette et al., 2009 [20] | Niet-neurogene OAB, vrouwen | 37 | PTN (NL) | - | - | - | 8 S, 2/W, Schijngroep | Frequentie en urgentie verbeterden aanzienlijk in beide groepen | - |
Schreiner et al., 2010 [18] | UUI, de oudere vrouwen | 51 | PTN (NL) | 10 Hz | 200 ms | Enige motorische respons | 12 s, 1/w, 30 min, bediening | UUI aanzienlijk verbeterd in 76% Tegen 26,9% van de patiënten in de controlegroep | - |
de Seze et al. 2011 [19] | MISSEN | 70 | PTN (NL) | 10 Hz | 200 ms | Onder motorische respons | 3 m, 1 / dag, 20 min | 83,3% verbeterde de urgentie op basis van tijd, MHU-subschaal urgentie en waarschuwingsfrequentie | Geen totaal. van de patiënten detrusor hyperactiviteit (86%) significant gedaald tot 73% |
Booth et al. 2013 [45] | Blaas / Erectiele Darm, Ouderen | 30 | PTN (NL) | 10 Hz | 200 ms | Comfortniveau | 12 s, 2/w, 30 min, schijngroep | Frequentie: 74% Vs. 42% in nep | - |
DH, hyperreflexische detrusor; IC, interstitiële cystitis; IDI, idiopathische detrusorinstabiliteit; IDO, idiopathische detrusorhyperactiviteit; IVD, irriterende ledigingsstoornissen; MCC, maximale cystometriecapaciteit; MHU, Mesure du Handicap urinaire; MS, multiple sclerose; OAB, overactieve blaas; PTN, achterste scheenbeenzenuw; dwarslaesie, dwarslaesie; SU, zintuiglijke urgentie; UUI, urinaire aandrangincontinentie.
Tabel opties
Tabel 2.
Literatuurstudie van de acute urodynamische effecten van TENS.
Eerste jaar van auteurschap | Diagnose | n | Plaats | Impuls Parameters Stimulus | Details van het onderzoek | Urodynamisch resultaat | ||
Frequentie | Puls Breedte | Intensiteit | ||||||
Hasan et al., 1996 [12] | IDES | 36 | Suprapubische PTN | 50 Hz | 200 ms | kietelend gevoel | Onderdeel van het grote onderzoek | Geen significant verschil in een van de parameters |
59 | S 2 -S 3 T 12(schijnvertoning) Beheersen | 50 Hz | 200 ms | kietelend gevoel | 3 Groepen, Fictie, Controle | MCC significant verhoogd in S 2 -S 3 Stimulatie in vergelijking met schijnvertoning en controle | ||
Bower et al., 1998 [23] | VAN, AAN | 79 | sacraal | 10 Hz | 200 ms | Max. toelaatbare sensatie | 3 groepen, Sham | max. DP en FDV toename |
suprapubisch | 150 Hz | 200 ms | max. DP en FDV toename | |||||
fictie | Geen stimulans | toename van MCC naar Su pts. | ||||||
Walsh et al., 2001 [29] | IDI, SU, DH (SKI, MS) | 146 | Perianale dermatomen | 10 Hz | 200 ms | - | Controlegroep | FDV ( p = 0,002) en MCC ( p = 0,0009) is verbeterd ten opzichte van de |
Amarenco et al., 2003 [37] | MS, SCI, PD, IDI | 44 | PTN (NL) | 10 Hz | 200 ms | Onder motorische respons | Acuut effect | 48% (21/44) verhoogde volume bij FIDC, 34% (15/44) verhoogde MCC |
Fjorback et al., 2007 [30] | MISSEN | 12 | sacraal | 20 Hz | 500 ms | 50-60 mA | Voorwaardelijke stimulatie | 0/12 waren in staat om de samentrekking van de detrusor te onderdrukken |
DPN | 20 Hz | 500 ms | 50-60 mA | 10/12 waren in staat om samentrekking van de detrusor te onderdrukken | ||||
DH, hyperreflexische detrusor; DI, knik detrusor; DPN, dorsale penis/clitoriszenuw; FDV, eerste wens om te plassen; FIDC, eerste onwillekeurige samentrekking van de detrusorspier; IDI, idiopathische detrusorinstabiliteit; MCC, maximale cystometriecapaciteit; MS, multiple sclerose; PD, ziekte van Parkinson; PTN, achterste scheenbeenzenuw; dwarslaesie, dwarslaesie; SU, zintuiglijke urgentie.
Tabel opties
Tabel 3.
Samenvatting van onderzoeken beoordeeld op basis van hun type en plaats van stimulatie.
Geen controle | Placebo-controle | Andere vorm van controle | |
sacraal | Yokozuka et al. [11] | Bower et al. [23] | Fjorback et al. [30] |
PTNS (Kaartpunten) | Amarenco et al. [37] | Booth et al. [45] | Schreiner et al. [18] |
Suprapubisch / overig | Okada et al. [26] | Bower et al. [23] | Hasan et al. [12] |
Tabel opties
Om sacrale stimulatie te bereiken, Yokozuka et al. [11] Patiënten die de taak hadden om oppervlakte-elektroden op het achterste sacrale foramen te plaatsen en de intensiteit van de stimulatie tot een anale contractie te verhogen, konden worden gevoeld. Ze veronderstelden dat, in gevallen waarin er geen verbetering was, de elektroden niet in de juiste positie werden geplaatst of dat de intensiteit niet hoog genoeg was vanwege het bijbehorende ongemak. Er is steun voor Takahashi en Tanaka [38] waarbij kleine veranderingen in de positie van de elektroden merkbare schijnbare veranderingen in de urethrale drukrespons veroorzaakten [11] . De tot nu toe gerapporteerde sacrale stimulatieonderzoeken hebben meestal elektroden die in sacrale gaten of op de billen boven de S worden geplaatst 2 en S 3dermomen. De precieze plaatsing van elektroden op heilige plaatsen varieert tussen studies, vermoedelijk omdat de locatie van sacrale dermatomen onzeker is [39] en [40] . De intensiteit van de stimulatiestroom werd meestal ingesteld op een maximum dat werd bepaald door de pijngrens. In andere onderzoeken kregen patiënten de instructie om een intensiteit in te stellen die een kietelend gevoel veroorzaakte [12] , [14] en [15] . Zenuwstammen (wortels) in deze gebieden bevinden zich diep in foramina en het is onwaarschijnlijk dat deze direct werden gestimuleerd op het niveau van intensiteit van de gebruikte stimulus. De huidzenuwen in dermatomen zijn echter gemakkelijk te stimuleren en daarom kan oppervlakkige sensorische vezelstimulatie, die kan leiden tot zowel directe als indirecte modulatie van ruggenmergreflexmechanismen, de gerapporteerde effecten verklaren. Bovendien is de intensiteit die samentrekking van de anale sluitspier veroorzaakt [11] Het gaat om de stimulatie van de motorische zenuwen, waardoor verschillende mechanismen worden geactiveerd, en kan inderdaad aanzienlijk ongemak veroorzaken bij patiënten. Verduidelijking van de exacte plaats van stimulatie en de vereiste intensiteit moet in toekomstige werkzaamheden aan de orde komen. Op basis van het beschikbare bewijs kunnen we niet concluderen wat de beste stimulatieparameters zijn om te gebruiken voor sacrale stimulatie. De oorspronkelijke beschrijving van PTNS door McGuire et al. [16] Het werd niet herhaald in termen van de positie van de elektroden. De meeste studies plaatsen de elektroden in de buurt van de mediale malleolus, waar de PTN relatief ondiep is. Het is onduidelijk op welke poot de elektroden moeten worden geplaatst voor een optimale respons, en of dit belangrijk is; Sommige auteurs plaatsten elektroden op het linkerbeen [17] , [20] en [37] , terwijl anderen op het rechterbeen [18] , [19] en [31] . Het kan ook effectiever zijn voor het bilateraal plaatsen van elektroden, hoewel dit nog niet door studies is onderzocht. Bij het beschrijven van de huidige intensiteitsinstelling presenteerden sommige onderzoeken motorische reacties tijdens stimulatie [17] en [18] . In andere onderzoeken werd de stimulatie-intensiteit ingesteld op net onder de motorische drempel [37] of net boven de drempel van de waarneming [19] .
De studie die de meest veelbelovende therapeutische resultaten rapporteert, is die van de Seze et al. [19] , die PTNS-succes heeft gerapporteerd voor OAB-symptomen bij MS-patiënten. De stimulatie-intensiteit in deze studie werd vastgesteld achter de perceptiedrempel en patiënten rapporteerden geen motorische reacties na stimulatie. Dus alleen sensorische vezels of huidzenuwen die boven de PTN liggen, werden waarschijnlijk gestimuleerd, wat suggereert dat dit voldoende kan zijn voor de behandeling van OAB. Als de behandeling zelf wordt toegediend, is het waarschijnlijk dat de patiënt de voorkeur geeft aan lagere stimulatieniveaus, wat vervolgens kan leiden tot stimulatie van alleen de huidzenuwen in plaats van de achterste tibialiszenuw zelf.
4.2. Sham Stimulatie Methodologie
Onderzoek naar mogelijke placebo-effecten is waarschijnlijk essentieel bij de studie van nieuwe therapieën en dit is vooral het geval bij elektrische stimulatietechnieken vanwege de sensaties die ze veroorzaken. Vanwege deze sensaties kan de productie van schijn-elektrische stimulatie echter moeilijk zijn. Een interessante methodologie werd uitgevoerd in een onderzoek bij kinderen met OAB, waarbij in één arm van het onderzoek stimulatie werd toegepast over het schouderblad, waar effecten op de controle van de lagere urinewegen zouden worden verwacht [41] . Zo ook Hasan et al. [12] TENS toegepast over de T 12 dermatoom dat als placebo fungeerde.
Elektrische stimulatie onder motorische drempelniveaus veroorzaakt tintelingen als gevolg van stimulatie van de sensorische zenuwstructuren van de huid. Een alternatieve optie voor een schijnmethode kan zijn om de stimulatie-intensiteit na een paar seconden gebruik geleidelijk tot nul te verlagen en de proefpersoon aan te geven dat de sensatiestimuli na verloop van tijd kunnen vervagen. Dit is een benadering die veel wordt gebruikt in technieken zoals transcraniële stroomstimulatie [42] . Bovendien kan de proefpersoon zich aanpassen aan dergelijke stimuli dat ze niet echt in staat zijn om te herkennen of de stimulatie aanhoudt of niet. Deze gewenning hangt waarschijnlijk af van de frequentie van de gebruikte stimulatie, de sterkte van de toegepaste stimuli en van persoonlijke subjectieve reacties.
Een andere benadering bij onderzoek naar placebo-effecten zou kunnen zijn om elektroden op hetzelfde deel van de huid aan te brengen, maar zonder stimulatiestroom met behulp van stimulatoren die voor dit doel zijn aangepast [43] . Dit veronderstelt echter dat de patiënt naïef moet zijn over elektrische stimulatie en dus zonder te weten dat het sensatie veroorzaakt.
Leroi et al. [44] Voerde een gerandomiseerde schijngecontroleerde studie uit waarin patiënten niet werd verteld dat ze de schijnstimulatie konden krijgen. Patiënten werden gerandomiseerd in actieve en schijnstimuligroepen. Deze methodologie werd goedgekeurd door hun lokale ethische commissie, hoewel de redacteuren van het tijdschrift waarin ze vervolgens worden gepubliceerd, onderzoekers sterk afraden om een dergelijke methodologie te gebruiken, omdat ze dachten dat het een schending van de Verklaring van Helsinki zou kunnen betekenen. Wij zijn van mening dat dit een gerechtvaardigde aanpak is om de technische problemen op te lossen van fictieve stimuli die eraan worden onderworpen in het stadium van goedkeuring door de bevoegde ethische commissie. Er moet echter rekening worden gehouden met het voordeel voor de patiënt van een dergelijke regeling, en het aanbod van actieve behandeling na het onderzoek zou dit probleem kunnen aanpakken.
5. Conclusie
De keuze van de stimulatieparameters, de locatie van de toegepaste stimulatie, de gebruikte uitkomstmaten en de bestudeerde onderliggende aandoeningen en symptomen zijn tot nu toe zeer verschillend in de literatuur. Er zijn weinig follow-upgegevens op lange termijn gepubliceerd in de literatuur en daarom is het behandelingsregime om blijvende voordelen te produceren onduidelijk.
De huidige consensus is dat de meest veelbelovende plaats van stimulatie S is 3 gebied van het ruggenmerg op het sacrale gebied of boven de achterste scheenbeenzenuw, maar het is onduidelijk welke benadering van stimulusafgifte het meest effectief is. Er is weinig bekend over de mechanismen die ten grondslag liggen aan de werking en dat exacte structuren moeten worden gestimuleerd.
Er is echter verleidelijk bewijs voor de werkzaamheid van de transcutane stimulatiebenadering, hoewel verdere grote placebogecontroleerde onderzoeken nodig zijn om een solide kennisbasis te bieden. De standaardisatie van toekomstige procesmethodologie is belangrijk om vergelijkingen te kunnen maken tussen studies en stimulatieprotocollen.
Specificaties:
- Voeding: 2 x 1,5 V AA alkaline batterijen (LR6);
- Uitgang: 100 mApp bij 1000 Ohm belasting (met 200mS pulsen)
- Pulsbreedte: 50mS tot 400mS instelbaar in stappen van 50mS
- Frequentie: 1Hz tot 150Hz (1-2-3-4-5-10-12-14-16-18-20-25-30-35-40-45-50-60-70-80-90-100-110-120-130-140-150).
- Golfvorm: symmetrische bifasische pulsen - afwisselende bifasische pulsen.
- Behandelingstimer: Continu, 10min, 20min, 30min, 45min, 60min, 90min.
- ACTIE-/PAUZETIJDEN: Van 1 tot 60 sec, instelbaar in stappen van 1 sec.
- RAMP-tijd: Van 0 tot 5 sec, instelbaar in stappen van 1 sec.
- Afmetingen: 138 mm x 6 8 mm x 28 mm.
- Gewicht: 160 g batterijen inbegrepen.
- Bedrijfs- en opslagtemperatuur: van +5 tot +35 °C.
- Relatieve vochtigheid van gebruik en opslag: van 20% tot 80%.
Uitrusting:
- Intellistim BE-28UG-apparaat
- 2 stylusbatterijen
- Aansluitkabels
- gebruikershandleiding in het Engels
- Reisetui
Sondes moeten apart worden aangeschaft.
Perineale incontinentie elektrostimulator Beac IntelliSTIM BE-28UG
- Meer dan 90.000 tevreden klanten sinds 2020
- Veilige betalingen: creditcard, PayPal en bankoverschrijving
- Snelle verzending: Post en BRT
- Klantenservice Whatsapp +39 371 43 61 201
Andere vergelijkbare producten:

Reserveonderdelen en accessoires:

Anale sonde Chattanooga Saint-Cloud
BEAC anale sonde

BEAC Periprobe-2STW vaginale sonde

BEAC Perisphera vaginale sonde - AT met 4 elektroden

BEAC Perisphera vaginale sonde - H met 4 elektroden

BEAC Perisphera vaginale sonde - U met 4 elektroden

Draadelektroden voor Elektrostimulatie en Tens 50x50 - 4 stuks.

Paar kabels voor BEAC-elektrostimulatoren
- chevron_left
- 1
- 2
- 3
- 4
- 5
- chevron_right
Uw beoordelingswaardering kan niet worden verzonden
Rapporteer reactie
Melding verzonden
Uw opmerking kan niet worden verzonden
Schrijf uw recensie
Beoordeling verstuurd
Uw beoordeling kan niet worden verzonden